서 론
고령화가 전 세계적으로 가속화됨에 따라, 노인의 근감소증(sarcopenia)은 신체 기능 저하, 낙상, 장애, 그리고 삶의 질 감소를 유발하는 중대한 보건 문제로 주목받고 있다. 근감소증은 주로 단백질 합성 감소, 염증 증가, 호르몬 변화, 장내미생물 불균형, 미토콘드리아 기능 저하 등 복합적인 병태생리 기전으로 인해 발생하며, 이를 조기에 예방하거나 개선하는 것은 건강한 노화를 위한 중요한 대비책 중 하나이다[1]. 현재까지 근감소증을 예방하기 위한 접근으로는 저항성 운동과 단백질 보충이 가장 대표적이며, 다양한 기능성 영양소와 생리활성 성분을 활용한 식이 전략이 병행될 때 그 효과가 강화된다고 보고한다[2]. 특히, 유제품(dairy foods)은 고품질 단백질(유청, 카제인), 칼슘, 비타민 D뿐만 아니라, 락토페린, 유청 펩타이드 등 근육 대사에 긍정적 영향을 주는 영양 및 생리활성 성분을 다수 함유하고 있어 근감소증 예방에 효과적인 식품군으로 주목받고 있다[3,4]. 최근에는 유제품의 아미노산 구성 및 mTOR(mammalian target of rapamycin) 경로 자극 효과, 근세포 분화 유도 및 근위축 억제 효과[5], 장내미생물 조절을 통한 항염증 작용[6], 미토콘드리아 기능 보호에 대한 연구[7] 등이 보고되었다. 또한 최근 우유 유래 엑소좀의 분자기전 등이 다수의 연구를 통해 보고되고 있으며, 이러한 내용은 근감소증을 기전 중심으로 이해하고 실질적 예방 전략으로 연결하는 데 큰 기여를 하고 있다[8-10]. 이에 본 리뷰는 유제품이 고령자의 근감소증 예방과 개선에 기여할 수 있는 영양학적 및 생물학적 기전을 통합적으로 고찰하고, 임상 및 역학 근거를 바탕으로 고령자 맞춤형 유제품 섭취 전략을 제시함으로써, 근감소증 예방을 위한 실용적 식이 전략 수립에 과학적 기반을 제공하고자 한다.
본 론
골격근량의 조절은 단백질 합성과 분해 간의 균형을 담당하는 다양한 세포 내 신호전달 경로에 의해 이루어지며 Fig. 1에서 제시하였다. 이 중 mTOR은 근육 단백질 합성 조절의 핵심적인 serine/threonine kinase로, 기능적·구조적으로 구분되는 두 가지 복합체인 mTORC1(mTOR complex 1)과 mTORC2(mTOR complex 2)의 형태로 존재한다. 특히 mTORC1은 근육 단백질 합성 조절의 중심 경로로 작용하며, 성장인자, 아미노산(특히 류신[leucine]), 기계적 자극 등 다양한 상위 신호에 의해 활성 조절된다[11,12]. 저항성 운동은 수용체 매개 PI3K–Akt 신호전달 경로를 활성화하여 TSC1/2 복합체를 억제함으로써 mTORC1 활성을 유도하며, 동시에 integrin–PI3K–PDK1–Akt 경로를 통해 근섬유막 수준에서 mTORC1 신호를 촉진하는 것으로 알려져 있다[12-19]. 아미노산은 Rag GTPases–Ragulator 복합체를 통해 mTORC1을 리소좀 막으로 이동시켜 Rheb 의존적으로 활성화한다. 이 과정에서 Sestrin2는 세포질 내 leucine 감지자로 작용하여 GATOR2 억제를 해제함으로써 mTORC1 활성을 유도하며, arginine 감지는 CASTOR1을 통해 조절된다[20,21]. 하위 신호전달 단계에서 mTORC1은 p70S6K1과 4E-BP1을 인산화하여 eIF4F 복합체 형성을 촉진하며, S6K1 활성화와 4E-BP1 억제 해제를 통해 5’-cap 의존적 mRNA 번역을 증가시킨다[22]. 또한, mTORC1은 ULK1 인산화를 통해 자가포식을 억제하고, UPS(ubiquitin–proteasome system)을 간접적으로 조절함으로써 단백질 항상성 유지에 기여한다[23]. 이러한 일련의 기전은 세포 내 단백질, 지질, 핵산 생합성을 촉진하며, 특히 MyHC(myosin heavy chain) 등 근원섬유 단백질 합성을 유도한다(Fig. 1).
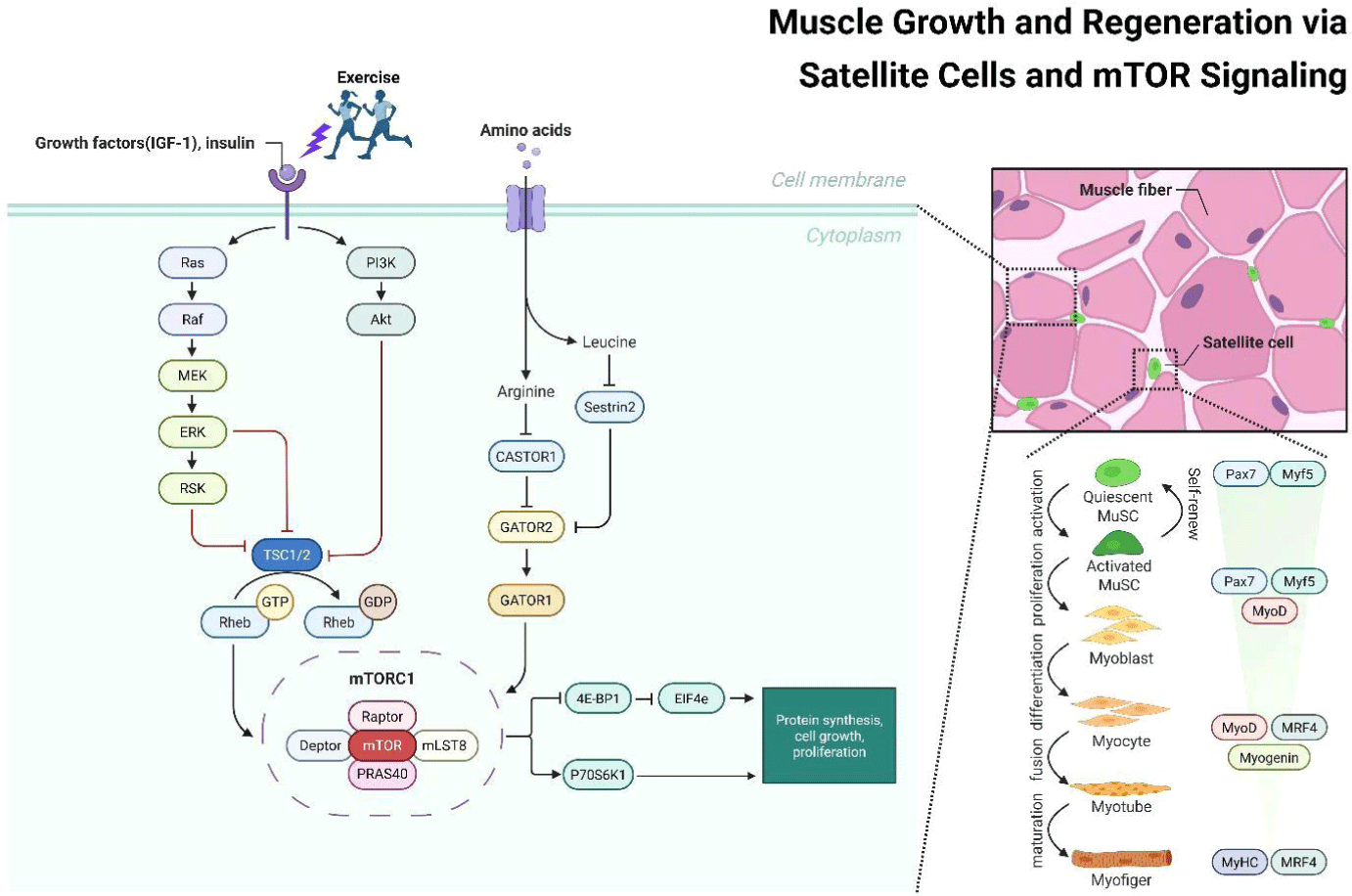
특히 유청 단백질과 카제인은 노인 대상 인체적용 연구에서 근육 단백질 합성을 유의적으로 촉진하는 것으로 다수 보고되었다[24,25]. 그러나 노화 과정에서 기저 mTORC1 활성이 증가함으로써 근육의 동화 반응이 둔화되는 ‘동화 저항성(anabolic resistance)’이 발생할 수 있다는 보고도 존재한다[11,26,27]. BCAA 중 leucine은 근육 단백질 합성 개시에서 가장 핵심적인 아미노산으로 알려져 있으며, 운동과 병행한 leucine 또는 leucine-rich 단백질 섭취는 동화 저항성 극복 및 근감소증 예방에 효과적인 전략으로 제시되고 있으며, 운동과 병행한 leucine 또는 leucine-rich 단백질 섭취는 동화 저항성 극복 및 근감소증 예방에 효과적인 전략으로 제시되고 있다[25,28]. Leucine 섭취는 운동과 병행 시 아나볼릭 저항성 극복과 근감소증 예방에 효과적이다[25,28]. 유청과 카제인은 leucine 함량이 높아 mTORC1을 강하게 자극하며, 두 단백질을 함께 섭취할 경우 유청의 빠른 흡수 특성과 카제인의 지속적인 아미노산 공급 특성이 상호 보완적으로 작용하여 근육 단백질 합성 반응을 장시간 유지하는 데 기여할 수 있다[29-31].
골격근은 체내 에너지 대사와 신체 움직임을 담당하는 핵심 조직이며, 미토콘드리아는 ATP 생성뿐만 아니라 지방산 산화와 아미노산 대사를 조절하는 중심 세포소기관이다[32]. 그러나 노화 및 근감소증 과정에서는 미토콘드리아 생합성과 산화적 인산화 능력이 저하되고, 활성산소종(reactive oxygen species, ROS)이 축적되어 근섬유 소실과 근력 저하가 유발된다[33]. 특히 미토콘드리아 품질 관리(mitochondrial quality control) 기전인 융합(fusion), 분열(fission), 미토파지(mitophagy)가 손상될 경우 미토콘드리아 기능 저하는 가속화되며, 이는 단백질 분해 경로 활성화와 근위축 관련 유전자 발현 증가로 이어진다[32]. 더불어 미토콘드리아 기능 저하는 염증 및 산화 스트레스 신호를 활성화하여 노화 관련 만성 염증 상태를 유도하고, 결과적으로 근단백질 항상성을 붕괴시킨다[33-35]. 따라서 미토콘드리아 기능 보존은 노화 관련 근감소증 예방 및 개선을 위한 핵심 전략으로 제시되고 있다.
최근 유제품 유래 생리활성 물질은 미토콘드리아 기능을 보호하고 근육 건강을 유지하는 중요한 영양 인자로 주목받고 있다. 일부 연구에서는 유제품 유래 성분이 UCP2 신호를 활성화하여 산화 스트레스를 억제하고, 미토콘드리아 호흡 효소 활성과 막전위를 회복시켜 조직 손상을 완화한 것으로 보고되었다[36]. 또한 lactoferrin과 대두 단백질 가수분해물을 혼합한 소재는 Keap1/Nrf2/HO-1 경로 및 PGC-1α 발현을 증가시켜 항산화 효과를 나타내었으며, 근육과 간의 글리코겐 축적 및 항피로 효과를 유도하였다[37]. Lactoferrin은 노화 관련 모델에서 항산화 및 항염증 효과를 보이며, 주요 수명 관련 신호 경로 조절을 통해 세포 노화 억제에 기여하는 것으로 보고되었다[38].
유청 유래 펩타이드 또한 미토콘드리아 항상성 유지에 긍정적인 영향을 미치는 것으로 알려져 있다. Acetaminophen 유도 간 손상 모델에서 whey protein hydrolysate는 ROS 축적과 NLRP3 inflammasome 활성을 억제하고, PINK1–Parkin 경로를 통한 미토파지 촉진으로 손상된 미토콘드리아 제거를 유도하였다[39]. 더 나아가 lactoferrin과 유청 단백질은 장 상피세포에서 지질 과산화와 단백질 카르보닐화 반응을 억제하고 TLR4 발현을 감소시켜 산화 스트레스와 염증 반응을 동시에 조절하는 효과를 나타냈다[40]. 이와 같이 유제품 유래 생리활성 물질은 Nrf2–HO-1 경로 활성화, PGC-1α 자극, 미토파지 유도 등 다양한 기전을 통해 미토콘드리아 기능을 보호함으로써, 궁극적으로 노화에 따른 근육 기능 저하와 근감소증 진행을 완화하는 데 기여할 수 있다.
운동이나 영양 자극은 단백질 합성을 촉진하여 근섬유 비대를 유도하는 반면, 암, 감염, 노화와 같은 이화성 자극은 단백질 분해를 활성화하여 근위축을 초래한다. 따라서 근단백질 합성(muscle protein synthesis, MPS)과 함께 근형성 촉진 및 근위축 억제는 근감소증 예방과 개선을 위한 핵심 조절 기전으로 간주된다[14]. 근형성 과정에서 myogenin은 분화 단계에서 근아세포(myoblast)를 성숙한 근세포(myocyte)로 전환시키고, MyHC 발현과 함께 다핵 근섬유 형성을 유도하는 주요 전사인자이다[41]. 위성세포(satellite cell)는 성인 골격근의 주요 줄기세포로서 근손상 후 근섬유 재생과 근핵(myonuclei) 보충에 핵심적 역할을 하지만, 노화가 진행됨에 따라 위성세포 풀(pool)의 감소와 기능 저하가 발생하며, 이는 근재생 능력을 제한하는 근감소증의 중요한 병태생리적 원인으로 작용한다[42].
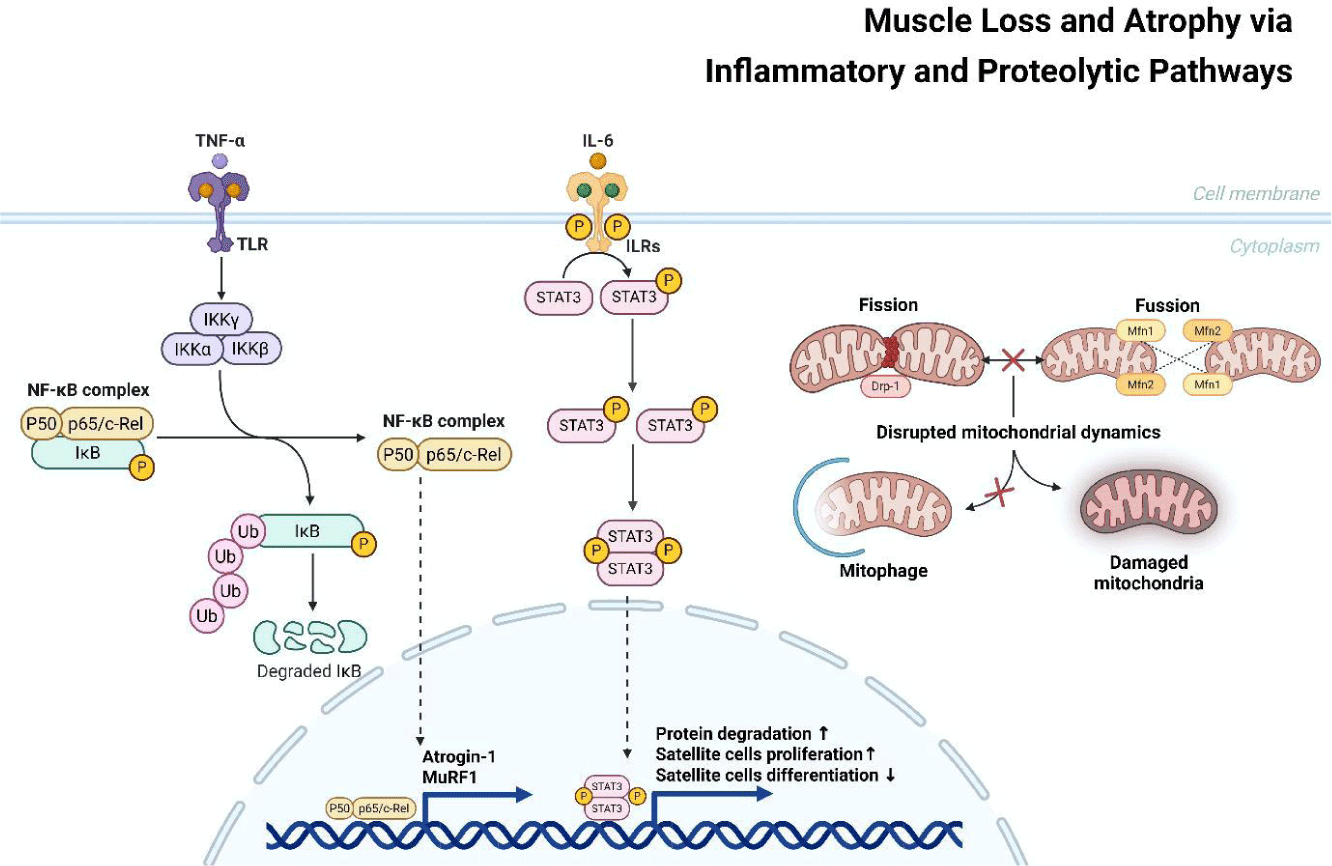
근위축은 근형성 능력 저하와 함께 단백질 분해 경로의 활성화로 특징지어지며, 대표적으로 UPS의 E3 ligase인 Atrogin-1/MAFbx와 MuRF1은 근육 구조 단백질을 분해하거나 성장 관련 신호를 억제함으로써 근위축을 촉진하는 핵심 조절 인자로 알려져 있다. 특히 노화나 만성 질환 상태에서는 이러한 이화성 신호가 미토콘드리아 기능 이상 및 염증성 사이토카인 신호가 결합되어 근위축이 더욱 심화되어 근손실을 가속화한다[14](Fig. 2).
반면 우유, 치즈, 요거트 등 유제품에 풍부한 칼슘과 비타민 D는 근육, 신경 및 골격 건강을 동시에 조절하는 필수 영양소로, 근감소증 예방 및 관리에 중요한 역할을 한다. 칼슘은 신경근 접합부에서 시냅스 소포 융합과 신경전달물질 방출을 매개하여 신경 자극을 근섬유 수축으로 전환시키는 데 필수적이며[43,44], 세포 내 칼슘 항상성은 정상적인 근수축과 신경전달 유지에 핵심적인 요소이다. 비타민 D는 장내에서 칼슘과 인의 흡수를 촉진하고[45], 골 무기질화를 유지할 뿐만 아니라 근육에서 mTOR 및 IGF-1 신호전달을 활성화하여 단백질 합성과 분화를 촉진하는 것으로 보고되었다[46]. 또한 MyoD와 myogenin 발현을 증가시켜 근위축 상태에서의 근육 회복을 보조한다. 반대로 비타민 D 결핍은 부갑상선호르몬(parathyroid hormone) 분비 증가를 유도하여 골 손실과 근력 저하를 초래하고, 노인의 낙상 및 골절 위험을 증가시키는 것으로 알려져 있다[45,47]. 종합적으로 볼 때, 칼슘과 비타민 D는 골–근육 단위(bone–muscle unit)의 항상성 유지에 핵심적인 조절 인자이며, 균형 잡힌 섭취는 근감소증뿐만 아니라 골다공증 예방과 건강한 노화를 위한 중요한 영양 전략으로 제시될 수 있다.
성인 장내미생물총은 Bacteroidetes와 Firmicutes가 우점하는 복합 생태계로, 면역 조절, 에너지 항상성, 영양 상태 및 전신 건강 유지에 핵심적인 역할을 수행한다[48,49]. 장내미생물은 탄수화물, 단백질 및 지질을 분해하여 숙주 대사에 필요한 에너지를 공급하며, 이 과정에서 생성된 미생물 대사산물은 장 장벽을 통과해 전신 순환으로 이동하여 다양한 조직 기능에 영향을 미친다[50]. 이 중 lipopolysaccharide와 trimethylamine N-oxide는 전신 염증을 유도하는 반면, SCFAs(short- chain fatty acids)와 담즙산은 숙주 대사 및 면역 항상성 조절에 기여한다[51].
노화 과정에서는 장내미생물 불균형(dysbiosis)이 발생하여 미생물 다양성과 유익 대사산물이 감소하고, 이는 근기능 저하와 밀접하게 연관된다[52]. 장 장벽 기능 저하로 인한 endotoxemia는 NF-κB 경로를 통해 TNF-α와 IL-6과 같은 염증성 사이토카인 분비를 증가시켜 근단백질 합성을 억제하고 분해를 촉진한다[53]. 반면 SCFAs는 항염증 및 면역조절 효과를 나타내며, AMPK 신호를 통해 에너지 대사를 개선함으로써 MPS에 긍정적인 영향을 미친다[54]. 또한 장내미생물은 아미노산 및 비타민 대사를 조절하여 근육 대사에 간접적으로 기여한다[52]. 예를 들어 tryptophan은 IGF-1/ p70S6K/mTOR 경로를 활성화하여 근섬유 합성 관련 유전자 발현을 촉진하며[54,55]. Lactobacillus와 Bifidobacterium은 엽산, 비타민 B12, 비타민 K와 같은 수용성 비타민을 합성하여 전신 순환을 통해 근기능 조절에 관여한다[56,57]. 이러한 맥락에서 유제품은 장내미생물과 근육 건강을 연결하는 핵심 식이 요인으로 주목받고 있다. 우유 단백질(카제인, 유청 단백질)은 MPS를 촉진하는 고품질 단백질 공급원일 뿐만 아니라, 장내미생물 조성을 유리하게 변화시키는 것으로 보고되고 있다. 특히 요거트, 케피어와 같은 발효유제품은 Lactobacillus 및 Bifidobacterium과 같은 유익균을 직접 공급하며, 이들 미생물이 생성하는 SCFAs와 비타민은 장–근육 축(gut–muscle axis)을 통해 항염증 효과와 근대사 개선 효과를 나타낸다[58,59]. 일부 인체적용 연구에서는 발효유 섭취가 노인에서 피로 감소, 악력 개선 및 근기능 유지에 기여한 것으로 보고되었다[60]. 따라서 발효유를 포함한 유제품 기반 영양 중재는 장내미생물 개선과 근육 건강 유지를 동시에 달성할 수 있는 유망한 전략으로 평가된다.
우유 유래 엑소좀(milk derived exosomes)은 단백질, 지질, microRNA 등 다양한 생리활성 인자를 포함하고 있으며, 면역 조절, 항염증 작용, 장내미생물 균형 유지 및 골대사 촉진 등 다양한 생리적 기능에 기여하는 것으로 보고되고 있다[61-64]. 지금까지의 연구는 주로 소 유래 우유 엑소좀을 중심으로 수행되어 왔으나, 최근에는 모유(human breast milk) 유래 엑소좀 또한 근육 성장 및 대사 조절과 연관된 생리적 잠재력을 지닌 것으로 보고되었는데, 근세포에서 Akt–mTOR–p70S6K 신호 활성과 연관된 단백질 합성 증가 및 근육 성장 촉진 효과를 나타내었으며, 이는 우유 엑소좀의 근육 동화(anabolic) 기능 가능성을 뒷받침하는 근거로 제시된다[65]. 한편, 소 유래 우유 또는 유청 단백질 기반 엑소좀/EV 연구에서도 C2C12 근관 모델을 중심으로 단백질 합성 증가, 근섬유 직경 확장 및 근분화 촉진과 같은 긍정적인 결과가 반복적으로 보고되었다.
최근 연구에서는 한편 최근 연구에서는 소 초유 유래 엑소좀(bovine colostrum-derived exosomes, BCE)이 근육 항상성 조절에 보다 뚜렷한 효과를 나타내는 것으로 보고되었다[8]. BCE는 근위축 유도 모델에서 Atrogin-1 및 MuRF1과 같은 근위축 관련 유전자 발현을 억제하고 근분화를 촉진하였으며, 선충 및 마우스 모델에서는 근구조 단백질 유전자 발현 증가와 함께 장내미생물 조성 개선 및 근육 대사 항상성 회복 효과가 관찰되었다. 특히 dexamethasone 유도 근위축 마우스 모델에서 BCE가 장–근육 축을 매개로 근대사 개선 효과를 나타냈다는 점은, 우유 엑소좀의 기능이 근육에 직접 작용하기보다는 장내미생물 및 대사 환경 조절을 통한 간접적 기전일 가능성을 시사한다. 최근 Li et al.(2025)의 논문에서 우유 세포외소포체는 장 점막 장벽 보호, 염증 조절, 면역 항상성 유지에 관여함으로써 장 병태생리 조절에 중요한 역할을 할 수 있음을 제시하여, 장내미생물 및 면역세포와의 상호작용을 통한 치료전략 및 접근방법을 제시하고 있다[66].
또한 유청 단백질에서 유래한 엑소좀/세포외소포는 C2C12 근세포 모델에서 단백질 합성과 근세포 비대를 유도하는 것으로 보고되었다[67]. 다만 이러한 효과는 주로 in vitro 수준에서 확인되었으며, 노화 또는 근감소증 in vivo 모델에서의 기능적 유효성에 대해서는 추가적인 검증이 요구된다. 이처럼 우유 및 초유 유래 엑소좀은 근육 단백질 합성 촉진, 근위축 억제, 미토콘드리아 및 대사 항상성 조절 등 다양한 측면에서 근육 건강 개선 가능성을 제시하고 있으나, 현재까지의 연구는 주로 in vitro 또는 동물 모델에 국한되어 있으며, 인체 적용 연구는 매우 제한적인 수준이다. 그러나 이러한 in vitro 결과와 달리, 일부 in vivo 연구에서는 우유 엑소좀 섭취가 악력, 운동 수행 능력(rotarod), 근육 내 아미노산 농도 등 근기능 지표에 유의한 변화를 유도하지 못한 사례도 보고되어, 연구 결과 간의 불일치가 존재한다[10,68,69]. 이러한 차이는 실험 대상의 생리적 상태(성장기 vs 노화), 투여 기간 및 용량, 평가 지표의 민감도 차이에 기인할 가능성이 있으며[70,71], 우유의 처리 조건(시판 살균유, 초유, 원유 등)에 따라 엑소좀의 생리활성 성분 조성이 달라질 수 있다는 점에서 설명될 수 있다[62]. 특히 살균유에서 분리된 엑소좀은 초유 유래 엑소좀에 비해 생리활성이 상대적으로 낮은 것으로 알려져 있다[72]. 우유 유래 엑소좀은 근육 건강과 관련된 연구가 아직 제한적이고 결과가 일관되지 않으나, 최근 BCE 연구에서 근위축 억제 및 대사 항상성 회복 효과가 제시되면서 향후 근육 건강 분야에서의 연구 및 응용 가능성이 확대되고 있다.
노인성 근감소증 예방 및 개선을 위한 단백질 보충 전략에 대한 임상 연구는 지난 10여 년간 양적·질적으로 확대되어 왔으며, 특히 유제품 유래 단백질을 중심으로 한 무작위 대조 임상시험(randomized controlled trials, RCTs)과 장기 중재 연구가 다수 수행되었다[6,73-75]. Table 1은 유제품 단백질과 식물성 단백질을 대상으로 수행된 임상 및 역학 연구를 비교·정리한 것이다. 유제품 단백질은 장내 미생물 다양성 증가, 염증 관련 지표 개선, 그리고 leucine 농도 증가 및 MPS 촉진과 같은 긍정적인 효과가 다수의 RCT 및 코호트 연구에서 일관되게 보고되었다. 반면 식물성 단백질은 장내 미생물 조성 개선 효과는 일부 관찰되었으나, 급성 또는 단기 중재 연구에서 MPS나 leucine 관련 지표 개선 효과는 제한적인 것으로 나타났다. 이러한 결과는 단백질의 질적 특성, 특히 leucine 함량과 생체 이용률 차이가 임상적 근육 반응에 중요한 영향을 미칠 수 있음을 시사한다. 특히 유청 단백질 및 발효 유청 단백질은 높은 leucine 함량과 빠른 소화·흡수 특성으로 인해 MPS 자극 효과가 뛰어난 단백질원으로 주목받아 왔다. 다수의 임상 연구에서 유청 단백질 또는 유청 기반 보충제를 섭취한 노인군은 대조군에 비해 근력, 악력, 근육량, 그리고 단기 신체수행능검사(short physical performance battery) 점수에서 유의한 개선을 보였으며, 이러한 효과는 저항성 운동과 병행될 경우 더욱 강화되는 경향을 나타냈다[60,73,76]. 최근의 임상 연구들은 근육량 증가뿐만 아니라 기능적 지표(functional outcomes)를 주요 평가 변수로 포함시키는 방향으로 발전하고 있다. 즉, 근력과 근육량 변화에 더해 보행 속도, 균형 능력, 일상생활 수행능력, 그리고 낙상 위험과 같은 임상적으로 의미 있는 지표들이 함께 분석되고 있다[60,73]. 유제품 또는 유단백 보충은 근육 기능 유지와 신체 수행능 개선을 통해 노인의 신체적 취약성(frailty)을 완화하고, 장기적으로는 낙상 및 기능 상실 위험을 감소시킬 수 있는 영양 중재 전략으로 평가되고 있다. 한편 식물성 단백질을 활용한 임상 연구도 점차 증가하고 있으며, 대두 단백질 또는 두유 기반 중재 연구에서 일부 근육 관련 지표의 개선이 보고된 바 있다. 그러나 전반적으로는 MPS 자극 강도, 필수아미노산 및 leucine 함량, 그리고 임상 결과의 일관성 측면에서 유제품 단백질이 식물성 단백질보다 우수한 경향을 나타내는 것으로 평가된다[74,77]. 이러한 차이는 단백질 소화·흡수 속도, 필수아미노산 조성, 특히 leucine 함량의 차이와 관련된다. 따라서 현재까지 축적된 임상 연구 결과를 종합할 때, 유제품 단백질은 식물성 단백질에 비해 근육 합성 및 대사 관련 지표 개선 측면에서 보다 일관되고 우수한 효과를 나타내는 것으로 평가된다.
| Type of study | Protein | Participants | Duration | Key findings | Reference | |
|---|---|---|---|---|---|---|
| Dairy proteins | Systematic review (RCT) | Dairy products | Healthy adults, overweight/obese individuals, IBS patients, and other diverse conditions | 3–12 weeks | ↑ Bifidobacterium and butyrate-producing bacteria ↑ Gut microbiota diversity ↓ Inflammation-related markers; suppression of pathogenic bacteria |
[6] |
| Cohort | Dairy products | 21 countries, (n=147,812) | Long-term follow-up (average 9 years) | ↓ Incidence of hypertension Incidence of metabolic syndrome ↓ Incidence of diabetes |
[74] | |
| RCT | Whey protein | Healthy older adults (n=30) | Single session | ↑ MPS ↑ Blood leucine concentration |
[77] NCT01062711 | |
| Plant proteins | RCT | Soy milk | Overweight and obese men (n=17) | 4 weeks | ↑ Alpha diversity ↑ Bifidobacterium ↑ Lactobacillus |
[102] |
| RCT | Soy protein | Healthy older adults (n=30) | Single session | No increase in MPS ↓ Blood leucine concentration |
[77] NCT01062711 | |
우리나라 노인의 권장 칼슘 섭취량은 하루 800–1,000 mg이며[78], 하루 1컵의 우유 섭취가 권장되지만 실제 평균 섭취량은 319–457 mg으로, 권장량의 약 40%–80% 수준에 불과한 것으로 보고되었다[79]. 이는 국내 식생활에서 유제품 섭취 빈도가 낮고, 유당불내증 유병률이 약 75%로 높은 점과 관련이 있다[80]. 최근 50세 이상 활동적인 노인을 대상으로 한 연구에 따르면, 아침과 점심에 고단백 유제품을 섭취하고 점진적 저항성 운동을 병행할 경우 항염증성 사이토카인인 IL-10이 증가하면서 건강한 노년 남성에서 골격근량과 근력이 개선되는 것으로 나타났다. 또한 취침 전 40 g의 카제인 단백질 섭취는 수면 중 소화·흡수가 지속되어 이용률을 증가시키고, 수면 중 근원섬유 단백질 합성을 촉진하는 것으로 보고되었다[81]. 더불어 건강한 노년 여성에서 중등도 저항성 운동 중 유청 단백질 20–25 g을 보충한 경우, 운동 단독군에 비해 하지 근육량과 근력이 유의하게 증가하여 근감소증 예방에 효과적일 가능성이 제시되었다[82,83]. 따라서 노년층에서 유제품을 효과적으로 섭취하기 위해서는 아침과 점심 식사 시, 운동 직후, 그리고 취침 전과 같이 시간대별로 분산하여 섭취하는 전략이 바람직한 것으로 판단된다.
유제품은 골과 근육 건강에 필수적인 주요 영양소와 미량 영양소, 특히 칼슘의 섭취를 보장하는 중요한 식품이며, 비타민 D 강화 식품의 기질로도 활용될 수 있다. 예를 들어 치즈 30 g, 요거트 250 g, 또는 우유 250 mL에는 약 300 mg의 칼슘이 함유되어 있으며, 동일한 칼슘 섭취량을 비교하였을 때 유제품을 통한 섭취가 식물성 식품에 비해 골 및 근육 성장에 더 효과적인 것으로 보고되었다[84,85]. 그러나 한국 성인의 높은 유당불내증의 이유로 우유 섭취가 제한될 경우 칼슘, 인, 비타민 등의 섭취가 감소하여 미량영양소 결핍 및 예방 가능한 질환의 위험이 증가할 수 있다[86,87]. 이를 보완하기 위해 유당분해 우유, 발효유(요거트, 케피어 등), 무유당 제품의 섭취가 권장되며, 이러한 제품은 유당 함량을 낮추거나 유당불내증 증상을 완화하는 데 도움이 된다[88]. 프로바이오틱 요거트는 유당이 일부 분해되어 있어 유당불내증 환자도 비교적 쉽게 섭취할 수 있으며, 장내 유익균 유지에도 기여한다[58]. 유당불내증 환자에게는 우유를 다른 식품과 함께 섭취하거나, 하루 섭취량을 소량으로 나누어 식사 중 분산 섭취하고, 필요 시 외인성 락타아제를 병용하는 전략도 제안된다[89]. 빠르게 소화되는 유청 단백질 또는 동물성·식물성 단백질 혼합 섭취는 근육 보존에 효과적일 수 있으며, 액상 형태나 간식 형태의 보충도 실용적인 방법으로 활용될 수 있다. 또한 우유, 치즈, 발효유를 디저트나 간식으로 제공하는 것은 골 건강과 장내 균형 유지에 도움이 되며, 가격 접근성 개선이나 곡류·과일을 첨가한 발효유 제품은 지속적인 섭취를 유도할 수 있다[25,90]. 이와 같이 노년층에서는 유제품 섭취 시 섭취 시기, 섭취량, 제품 선택에 따른 맞춤형 전략을 통해 근육 및 골 건강 개선에 기여할 수 있다. 특히 유당불내증 비율이 높은 한국 노년층을 고려한 대체 제품 및 실질적인 섭취 전략은 중요하지만, 장기적 효과에 대한 검증 부족과 개인차에 따른 적용 한계라는 과제도 여전히 존재한다. 따라서 향후 연구에서는 한국 노년층을 대상으로 한 보다 표준화된 지표와 장기 추적 연구를 통해, 근육 개선을 위한 유제품 섭취 전략의 유효성과 안전성을 검증할 필요가 있다.
또한 노년층 근감소증 예방 전략에서 유제품을 식물성 단백질 및 대체 식품과 비교·평가하는 접근은 중요하다. 유제품은 leucine 함량이 높은 고품질 단백질을 제공하여 MPS 자극에 유리하며, 노년층에서 한 끼당 약 2.8–3 g의 leucine 섭취가 필요하다는 근거와도 부합한다[91,92]. 또한 칼슘과 비타민 D를 포함한 유제품 매트릭스는 근골격 건강을 통합적으로 지지할 수 있는 장점을 가진다[85]. 반면 식물성 단백질은 환경적 이점에도 불구하고, 필수아미노산 조성, leucine 함량, 소화·흡수 효율 측면에서 유제품 단백질에 비해 근육 동화 반응이 제한될 가능성이 보고되었다[93]. 이에 따라 노년층에서는 식물성 단백질 단독 섭취보다는 섭취량 증가, 단백질원 혼합, 또는 leucine 보강 전략이 필요할 수 있다. 최근 곤충 단백질, 배양육, 식물성 대체육 등 다양한 대체 식품이 제시되고 있으나, 제품 간 영양 조성과 가공 수준의 이질성이 커 건강 효과 해석에는 주의가 요구된다[94]. 특히 강화 두유는 일부 식이지침에서 유제품 대체 옵션으로 인정되지만, 대부분의 식물성 음료는 영양 동등성이 낮은 것으로 보고되었다[95]. 따라서 현 단계에서는 유제품을 노년층 근육 건강을 위한 근거 기반 핵심 식품군으로 유지하되, 개인의 건강 상태와 식생활 선호를 고려하여 식물성 단백질과 대체 식품을 보완적으로 활용하는 접근이 현실적인 전략으로 판단된다.
현재까지의 여러 연구에서 유제품 섭취가 근감소증의 예방 및 개선에 기여할 가능성이 제시되고 있으나, 연구 결과 간의 일관성 부족과 장기적 효과에 대한 근거 부재는 여전히 해결되지 않은 문제로 남아 있다. 지금까지 수행된 연구들은 대상자의 연령, 성별, 기저 질환 유무 등에서 차이를 보이며[85,96-98] 근기능 평가 역시 악력, 보행 속도, 근육량 등 서로 다른 지표를 사용하고 있다[98]. 또한 연구에 포함된 유제품은 우유 및 치즈[99], 발효 유제품[85,97], 유청 단백질[28,85] 등으로 그 종류가 다양하고, 영양 성분 조성, 섭취량, 섭취 기간 및 평가 기준 역시 연구마다 상이하여 결과 해석의 일관성을 저해하고 연구 간 비교 및 통합 분석을 어렵게 한다. 이러한 한계로 인해, 표준화된 평가 지표를 적용하고 비교적 동질적인 대상자군과 중재 조건을 설정한 고품질 연구가 요구된다. Table 2에서 제시한 바와 같이, 현재 대부분의 연구는 수 주에서 수 개월에 이르는 단기 중재에 국한되어 있어 장기적인 건강 효과 및 안전성을 평가하기 어렵고, 근감소증 예방 효과에 대한 근거 또한 충분하지 않다[75,85,97,99-102]. 게다가 고지방·고당 유제품의 장기 섭취가 대사질환 위험에 미치는 영향 역시 명확하게 규명되지 않았으며, 일부 포화지방산은 혈중 LDL 콜레스테롤 증가 및 심혈관질환 위험 증가와 연관될 가능성이 제기되고 있으나, 이에 대한 장기 관찰 연구는 제한적인 실정이다[85]. 반면, 발효유 및 저지방 유제품은 대사 지표 개선 및 심혈관 보호 효과를 나타낼 가능성이 제시되었으나, 유당불내증 인구를 포함한 장기적 안전성에 대한 데이터는 여전히 부족하다[103]. 이러한 근거를 종합할 때, 특정 인구집단을 대상으로 한 장기적 안전성 검증이 추가로 필요하다. 현재 연구에서는 동일한 개념을 서로 다른 방식으로 해석하거나 측정하는 등 근기능 및 바이오마커 평가에 있어 이질성이 존재한다[104]. 이러한 비표준화 상태는 연구 간 결과 비교 및 메타분석을 어렵게 할 뿐만 아니라, 조기 진단이나 중재 효과 평가에 활용할 수 있는 핵심 지표의 부재로 이어진다[98]. European Working Group on Sarcopenia in Older People 2는 ‘근력 감소’를 근감소증의 핵심 요소로 제시하고, 근력의 양과 질, 신체 수행능을 통합한 표준화된 평가 방법을 제안함으로써 지표 해석의 일관성을 높이고자 하였다[105]. 그러나 근감소증은 병태생리 기전이 복합적이기 때문에 단일 지표만으로 이를 충분히 설명하기에는 한계가 있으며, 근육량과 근기능 지표뿐 아니라 혈액 및 분자 수준의 바이오마커를 포함한 통합 지표 세트의 개발이 필요하다[96,98]. 따라서 향후 연구의 주요 과제는 근력 및 신체 기능과 같은 물리적 평가 지표와 분자·혈액 바이오마커를 병행하여 사용하되, 각 지표에 대한 표준화된 평가 방법과 해석 프로토콜을 확립함으로써 연구 간 이질성을 최소화해야 한다.
| Type of study | Participants | Treatment | Duration | Key findings | Exercise | References |
|---|---|---|---|---|---|---|
| RCT | Humans of any age, health status, or sex (n=907) | Fermented-milk kefir 100–800 mL/day | 10 days–6 month | ↓ Total cholesterol ↓ LDL cholesterol ↔ Bone mineral density |
☓ | [97] |
| RCT, quasi-experimental study | Older adults with sarcopenia≥60 years (n=854) | Nutritional supplementation (whey, protein, leucine, casein, milk, and soy) | 10–24 weeks | ↑ Grip strength ↔ 5-chair stand test ↔ gait speed |
○ | [101] |
| RCT, double-blind | Healthy older adults (60–84 year) (n=122) | Milk protein 10 g/day | 26 weeks | ↑Lean body mass ↔ Physical performance tests |
○ | [75] |
| RCT, double-blind | Middle-aged Korean adults (n=120) | Fermented whey protein | 8 weeks | ↑ Muscle strength ↑ Muscle mass ↑ Physical performance |
☓ | [73] |
| RCT, double-blind | Older adults with sarcopenia (n≈380) | Leucine-enriched protein | 13 weeks | ↑ Grip strength ↑ SPPB score |
☓ | [76] |
| Cohort | Korean adults aged≥50 years | Dairy product | Long-term follow-up (~10 years) | Maintained muscle mass and physical function ↓ Risk of sarcopenia |
☓ | [60] |
| RCT | Adults (total n=468) | Dairy product | 3–12 weeks | ↑ Lactobacillus ↑ Bifidobacterium ↓ Bacteroides fragilis |
☓ | [6] |
최근 한국인의 식생활은 전통적인 식단에서 서구화된 식단으로 변화하고 있으며, 과거에 비해 열량과 지방 섭취가 증가함에 따라 대사질환의 발생률 또한 증가하는 것으로 확인되고 있다[106-108]. 유제품 섭취를 포함한 식습관은 장내미생물의 구성을 변화시키고, 이는 대사 및 염증 경로를 통해 근육 건강에 직·간접적으로 영향을 줄 수 있다[109,110]. 또한 최근 연구에서는 CAV3, ACTN3, MTHFR 등의 유전자 변이와 호르몬 및 마이오카인 신호 변화가 근손실 위험을 증가시킬 수 있음이 보고되었다[110,111]. 특히 이러한 유전적 요인이 운동 부족, 비만, 흡연, 음주와 같은 환경적 요인과 결합될 경우 근기능 저하가 더욱 가속화되는 것으로 알려져 있다[96]. 그러나 현재까지 식습관, 유전적 요인, 그리고 근감소증을 하나의 경로로 직접 연결한 연구는 부족한 실정이다[96,98]. 또한 다른 단백질 공급원을 고려하여 최적의 영양 중재 전략을 설계하기 위해서는 유제품, 식물성 단백질, 그리고 대체 식품을 단순히 상호 대체 관계로 비교하기보다는, MPS 반응, 근기능 지표, 장내미생물 변화, 장기 안전성을 포함한 통합적 평가 틀 안에서 각각의 역할과 한계를 규명할 필요가 있다[109,111]. 특히 노년층에서는 단일 식품군에 의존하기보다, 개인의 소화 능력, 대사 상태, 유전적 특성, 생활 습관을 고려한 맞춤형 단백질 섭취 전략이 요구되며, 유제품은 이러한 전략에서 여전히 핵심적인 기준점(reference food)으로 기능할 수 있다. 궁극적으로, 다양한 단백질 공급원의 장점과 한계를 균형 있게 평가하는 연구가 축적될 때, 근감소증 예방을 위한 보다 실효성 높은 영양 중재 전략을 확립할 수 있을 것이다.
결 론
본 리뷰에서는 유제품 섭취가 노인의 근감소증 예방 및 개선에 기여할 수 있는 생물학적 기전과 임상 근거를 통합적으로 고찰하였다. 유제품은 leucine이 풍부한 유청 및 카제인 단백질을 통해 mTOR 신호전달 경로를 활성화함으로써 MPS를 촉진하며, lactoferrin, 펩타이드, 엑소좀과 같은 다양한 생리활성 성분은 근세포 분화 촉진, 근위축 억제, 산화 스트레스 완화 및 염증 조절을 통해 근육 건강 유지에 기여하는 것으로 보고되었다. 또한 발효유 및 유산균은 장-근육 축(gut–muscle axis)를 통해 장내 환경을 개선하고 근육 건강을 지지하는 역할을 수행한다. 최근 주목받고 있는 우유 유래 엑소좀에 대해서도 다수의 전임상 및 임상 연구에서 장내미생물 조절과 항염증 효과가 보고되었으며, 미토콘드리아 기능 유지에 긍정적인 영향을 미칠 가능성이 제시되었다. 이러한 기전적 근거를 바탕으로, 유제품 섭취는 근세포 성장 촉진 및 근위축 억제를 통해 근육 건강 개선에 기여할 잠재력을 지닌 것으로 판단된다. 한편 식물성 단백질과 대체 단백질 식품은 환경적·윤리적 측면에서의 장점으로 주목받고 있으나, 노년층 근감소증 예방 관점에서는 필수아미노산 조성, leucine 함량, 생체이용률 측면에서 유제품 단백질에 비해 근거가 제한적이다. 또한 가공 수준과 영양 조성이 다양한 대체 식품의 경우 근육 건강에 대한 효과를 일반화하기에는 임상적 근거가 충분하지 않다. 향후 연구에서는 유제품을 기준 식품군으로 하여 식물성 및 대체 단백질의 역할을 보완적 관점에서 비교·평가함으로써, 노년층을 위한 보다 정밀한 단백질 섭취 전략을 제시할 필요가 있다. 결론적으로, 유제품은 노년층에서 근감소증 예방과 건강한 노화를 위한 핵심적인 영양 전략이 될 수 있으며, 본 리뷰에서 제시한 통합적 분석은 향후 근육 건강 기능성 식품 개발, 임상 영양 중재 및 보건 정책 수립을 위한 기초 자료로 활용될 수 있을 것이다.






