ARTICLE
저온 캡슐화에 의한 Weissella cibaria CMU의 생존율 증진 효과
이다언1
,
황효정2
,
조유나1
,
정태환2
,
한경식1,2,*
Enhancement of Viability of Weissella cibaria CMU by Low-Temperature Encapsulation
Da-Eon Lee1
,
Hyo-Jeong Hwang2
,
Yu-Na Jo1
,
Tae-Hwan Jung2
,
Kyoung-Sik Han1,2,*
Author Information & Copyright ▼
1Department of Food Science and Biotechnology, Sahmyook University, Seoul, Korea
2Biomaterials Research Institute, Sahmyook University, Seoul, Korea
*Corresponding author : Kyoung-Sik Han, Department of Food Science and Biotechnology, Sahmyook University, Seoul, KoreaTel : +82-2-3399-1765. Fax : +82-2-3399-1655, E-mail :
kshan@syu.ac.kr
ⓒ Copyright 2018, Korean Society of Milk Science and Biotechnology. This is an Open-Access article distributed under the terms of the
Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0/) which permits
unrestricted non-commercial use, distribution, and reproduction in any
medium, provided the original work is properly cited.
Received: Sep 18, 2018 ; Revised: Sep 19, 2018 ; Accepted: Sep 19, 2018
Published Online: Sep 30, 2018
Abstract
In this study, we aimed to investigate the effects of low-temperature encapsulation on the viability of Weissella cibaria CMU under harsh conditions and in freeze-dried foods during storage. The capsules were prepared by gelation of sodium caseinate at different concentrations (5%, 6%, 7%, and 8%) with a combination of 0.5% gellan gum and 2% glucono-δ-lactone. The size distribution of the capsules was determined using a Mastersizer 3000 laser diffraction particle size analyzer. Scanning and transmission electron microscopy revealed that the capsule with 6% sodium caseinate had a smooth and rounded external surface, with reproducibility. The acid, bile, and heat tolerances of the encapsulated cells were significantly higher than those of the control under prolonged acid (5 h), bile (12 and 24 h), and heat (2 h) exposure, respectively. During storage for up to 6 months at 4℃ or 25℃, the viability of encapsulated Weissella cibaria CMU in beef and vegetable rice porridge was effectively improved.
Keywords: Weissella cibaria CMU; sodium caseinate; gellan gum; low-temperature encapsulation
서론
구강 건강은 인체 건강을 유지하기 위한 핵심적인 요소로 작용한다. 치아우식병과 치주질환은 우리나라 국민의 10대 만성질환에 포함되어 있으며, 국민건강보험 외래 진료건수 및 지출 순위 10위 안에 포함되어 있을 정도로 높은 비율을 차지하는 질환이다(Health Insurance Review and Assessment Service, 2016). 구강건강 문제는 구강기능 상태뿐만 아니라, 전반적인 건강상태나 사회성, 자신감 및 삶의 만족도와 밀접한 관련이 있다(Yoon et al., 2014; Choi et al., 2015; Chun and Lee, 2017). 이에 따라 구강 내 세균의 성장을 억제하면서 구강질환을 예방하기 위해 불소화합물, 자일리톨 껌, 스케일링, 항균치약 등과 같은 방법을 사용하고 있다(Park et al., 2010; Kim, 2017). 하지만 치아우식증 유발 세균을 억제하기 위해 가장 많이 사용되는 불소화합물은 과도한 섭취 시 복통과 반점치 및 암을 유발할 수 있으며(Spencer and Do, 2008), 껌이나 캔디 제형으로 제조 가능한 자일리톨의 경우, 일시적인 구취억제 효과는 충분히 기대할 수 있으나(Aluckan and Ankola, 2018), 제품이 닿지 않는 사각지대까지 제어할 수 없을 뿐더러 자일리톨은 하루에 상당한 양을 섭취해야 충치유발세균(Streptococcus mutans)의 생육이 억제 가능하다는 단점이 있다(Li and Tanner, 2015).
본 연구에서는 기존 구강 관리법의 문제점을 보완, 대체하기 위한 방법으로 구강 내에 정착하여 서식하면서 구취와 충치를 억제하고, 치주질환을 일으키는 다양한 유해세균를 선택적으로 제어할 수 있는 구강 프로바이오틱스(probiotics) 균주인 Weissella cibaria CMU 균주를 사용하였다(Jang et al., 2016; Kang et al., 2017; Do et al., 2018). 그러나 구강 건강 개선용 프로바이오틱스를 식품에 활용할 경우, 식품 가공 단계나 저장 기간 중에 활력의 소실이 발생할 수 있고, 특히 식품의 섭취 전 전처리 등에서도 활력 소실의 가능성이 있어 균주의 기능성 발휘에 대한 대안이 제시되어야 한다.
캡슐화 공법은 식품, 의약품 및 화장품 산업에서 널리 사용되고 있는 기법으로 특히 미생물의 생존율 향상에 적용되어 왔다(Iravani et al., 2015; Ansari et al., 2017). 현재 분무건조 및 고압균질기 등을 이용한 다양한 캡슐화 방법이 고안되어 왔으나, 일부 고온 처리 방식의 경우 유산균을 사멸시키는 부작용으로 인해 한계점을 갖게 되었다(Bae and Kim, 2008; Kim et al., 2013; Kim and You, 2017). 그러나 본 연구에서 사용된 저온 캡슐화 과정은 특정한 장비가 필요 없이 저온 상태에서 균주를 포집할 수 있는 기법으로 알려져 있다(Nag et al., 2011).
따라서, 본 연구에서는 균주의 안정성을 확보하고, 식품에 적용할 경우 보존성을 향상시킬 수 있는 효율적이며 저비용의 저온 캡슐화 방법을 사용하여 구강 프로바이오틱스의 활용성을 확대하고자 실험을 수행하였다.
재료 및 방법
1. 사용 균주 및 배양 조건
실험에 사용된 Weissella cibaria CMU 균주(이하 CMU 균주)는 (주)오라덴틱스에서 분양받아 37℃, 18시간 동안 최소 3번 계대 배양하여 사용하였다. 캡슐화에 사용할 균주 생산을 위해 1 L MRS 배지에 균주를 배양하고 5,000 rpm, 10분 동안 원심분리하여 균주를 회수한 다음, 0.1% peptone 용액으로 3번 세척한 후 20 mL peptone 용액에 희석하여 실험에 사용하였다.
2. 저온 캡슐화 공정
캡슐화 과정은 Nag(2011)의 방법을 일부 수정하여 실시하였다. 다양한 농도(5%, 6%, 7%, 및 8%)의 sodium caseinate와 0.5% gellan gum 혼합액(이하 혼합액)을 4℃에서 교반하면서 완전히 용해시켰다. 혼합액의 살균을 위해 90℃, 30분간 가열한 후 다시 38℃에 도달할 때까지 교반하며 온도를 낮춘 다음 농축된 유산균을 혼합액에 10:1 비율로 첨가하였다. 다시 2% glucono-δ-lactone(GDL)를 첨가한 다음, 혼합액의 pH가 5.5에 도달할 때까지 교반한 후 카놀라유에 약 5:1(카놀라유:혼합액) 비율로 혼합하고, 90분간 교반하며 캡슐을 형성시켰다. 카놀라유를 제거하고 형성된 캡슐은 0.1% peptone 용액에 3번 세척한 다음 4℃에 저장하며 사용하였다.
3. 캡슐의 크기 측정
Mastersizer 3000 laser diffraction particle size analyzer(Malvern Instruments, Malvern, UK)을 이용하여 다양한 농도의 sodium caseinate에 따른 캡슐의 크기를 측정하였다. 시료당 10번씩 반복 측정하여 입자 직경의 최소, 최대 및 평균값을 측정하였다.
4. 전자현미경 관찰
캡슐의 형상을 살펴보기 위해 주사전자현미경(SU-70, Hitachi, Tokyo, Japan)을 사용하였다. 데시케이터 안에서 캡슐의 수분을 제거한 후 carbon stub에 고정한 다음, SEM ion sputter coater를 이용하여 진공상태에서 60초간 도금하여 가속 전압 5k, 33 배율로 시료를 관찰하였다. 또한, Ann 등(2007) 의 방법에 따라 전처리를 통해 유산균 캡슐을 파쇄한 후 투과전자현미경(H-600, Hitachi, Tokyo, Japan)을 사용하여 캡슐 안의 유산균 포집 형상을 확인하였다.
5. 내산성, 내담즙성 및 내열성 측정
Minekus 등(2014)의 방법에 따라 캡슐화된 균주의 내산성을 측정하였다. KCl-HCl buffer(pH 2.0)에 pepsin 1,000 unit/mL를 첨가하여 인공위액을 제조하였으며, 이 용액 18 mL에 2 g의 시료를 첨가하고 37℃에서 shaking incubator로 교반하면서 0분, 2.5시간 및 5시간 동안 배양한 다음 0.1% peptone 수로 희석 후 MRS agar를 사용하여 37℃, 48시간 동안 혐기 배양하여 총균수를 측정하였다. 내담즙성 측정은 Nag 등(2011)의 방법에 따라 실시하였으며, monobasic potassium phosphate(0.68%, w/w)에 porcine bile extract(1.0%, w/w)을 첨가한 용액 18 mL에 2 g의 시료를 첨가하고 0시간, 12시간 및 24시간 동안 배양한 다음, 내산성에 사용된 동일한 방법으로 총균수를 측정하였다. 캡슐화된 균주의 내열성 평가는 Ann 등(2007)의 방법에 따라 실시되었으며, glycine-HCl buffer(pH 3.0) 18 mL에 2 g의 시료를 첨가하고 55℃ 항온수조에서 교반하면서 0시간, 1시간 및 2시간 후에 시료를 채취한 다음 상기한 방법에 따라 총균수를 측정하였다.
6. 저장 기간 중 동결건조식품 내 Weissella cibaria CMU의 생존율 조사
한우야채죽과 게살새우브로콜리죽 제품에 캡슐화된 Weissella cibaria CMU 균주를 첨가하여 동결건조시킨 다음, 다양한 온도(4℃, 25℃ 및 37℃)에 저장하면서 캡슐화하지 않은 CMU 균주를 첨가한 제품군(대조구)과 균주의 생존율을 비교, 조사하였다. 총 6개월 동안 1개월 간격으로 각 제품별 3개의 시료를 0.1% peptone 수와 stomacher를 사용하여 균일하게 환원시킨 다음, MRS agar로 37℃, 48시간 동안 혐기 배양시켜 기간에 따른 온도별 유산균 생존율을 측정하였다.
7. 통계분석
자료 분석은 SAS software(SAS version 9.2; SAS Institute Inc., Cary, NC, USA)를 사용하였으며, 내산성, 내담즙성 및 내열성은 초기균수 대비 시간별 생존율의 변화를 paired T-test를 사용하여 분석하였다(p<0.05).
결과 및 고찰
Sodium caseinate 농도(5%, 6%, 7%, 및 8%)에 따른 캡슐의 크기 분포를 측정한 결과, 각각 197∼1,170 μm(평균 632 μm), 620∼2,200 μm(평균 1,200 μm), 688∼1,300 μm(평균 944 μm) 및 169∼1,030 μm(평균 544 μm)로 나타났다. 캡슐화 과정은 압출, 유화 및 코아세르베이션 등 다양한 방법이 활용 가능하고 사용되는 시약 및 방법에 따라 캡슐의 크기 분포는 20∼4,000 μm로 다양하게 제조될 수 있다(Adhikari et al., 2003 ; Muthukumarasamy et al., 2006). Jung 등(2009)은 캡슐 제조시 크기뿐만 아니라, 안정성이 매우 중요하며, 캡슐의 크기 분포가 너무 작은 경우 제품 가공시 캡슐이 깨지는 등 취급에 어려움이 발생한다고 보고하였다. 본 연구에서 캡슐의 크기 분포는 sodium caseinate의 농도에 따라 169∼2,200 μm로 다양하게 제조되었고, 6% sodium caseinate 농도로 캡슐을 제조할 경우 다른 농도에 비해 상대적으로 캡슐이 안정적으로 형성되었으며, 재연성이 뛰어나 본 연구의 캡슐 제조를 위한 최종 농도로 선정하였다. 특히, 상대적으로 큰 입자의 캡슐은 동결건조에 의한 프로바이오틱스의 손실을 감소시켜줄 것으로 판단되며, 본 연구의 목적인 동결건조 죽 제품에 첨가시 식감에 어떠한 영향도 주지 않음을 알 수 있었다.
최종 확정된 캡슐 조성에 따라 6% sodium caseinate와 0.5% gellan gum으로 제조된 유산균 캡슐의 동결건조 후 형상과 균주 포집 상태를 SEM과 TEM 방법으로 관찰하였다. 캡슐의 표면을 관찰한 결과, 캡슐은 동결건조를 한 후에도 비교적 구형의 모양으로 원형을 유지하고 있었다. 수분 제거로 인해 mastersizer로 측정한 결과보다 다소 수축되어 있었으나, 매끄러운 표면이 관찰되는 것을 볼 때 동결건조에 의한 캡슐의 표면 손상은 발생하지 않은 것으로 판단되었다(Fig. 1A). 또한, 캡슐화된 균주를 파쇄하여 캡슐의 단면을 TEM으로 촬영한 결과, 캡슐에 포집되어 있는 CMU 균주를 확인할 수 있어 균주의 캡슐화가 성공적으로 이루어졌음을 확인할 수 있었다(Fig. 1B).
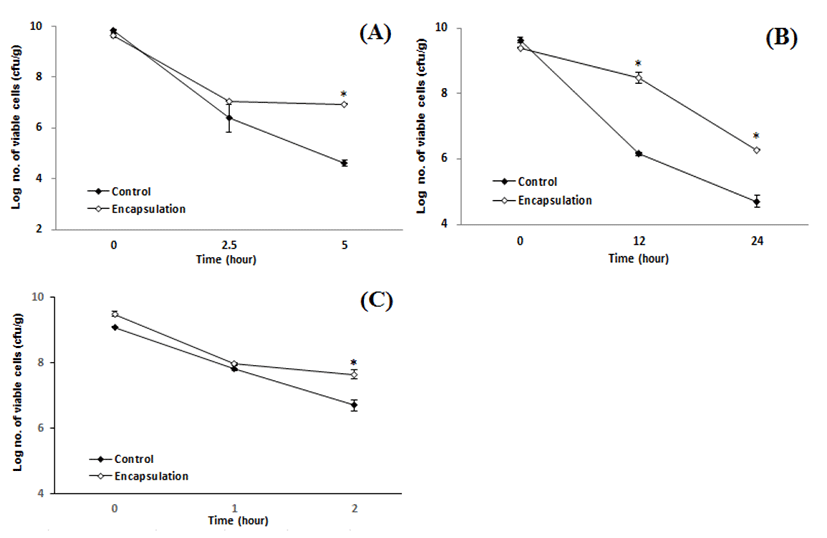
CMU 균주의 내산성을 조사한 결과, Fig. 2A에 나타난 바와 같이 대조구와 캡슐 모두 2.5시간동안 유의적인 차이를 보이지 않았지만, 5시간 동안 인공위액에 노출하였을 경우, 캡슐화된 균주가 일반 균주에 비해 유의적으로 높은 생존율을 보였다(p<0.05). 또한, 내담즙성 실험에서는 12 및 24 시간 동안 배양할 경우 캡슐화된 균주의 생존율이 대조구에 비해 모두 유의적으로(p<0.05) 높은 경향을 나타냈으며, 내열성의 경우, 55℃에서 1시간 동안은 생존율에 차이를 보이지 않았지만, 2시간 동안 가열할 경우 캡슐화된 CMU 균주의 생존율이 유의적으로(p<0.05) 높게 나타났다. 따라서, sodium caseinate(6%), gellan gum(0.5%) 및 GDL을 이용한 저온 캡슐화 기술은 산, 담즙 및 고온 등의 경쟁적인 환경에서도 CMU 균주의 생존율을 향상시킬 수 있음을 확인하였고, 이러한 보호 능력은 다양한 식품에 활용될 수 있을 것이라 판단된다.
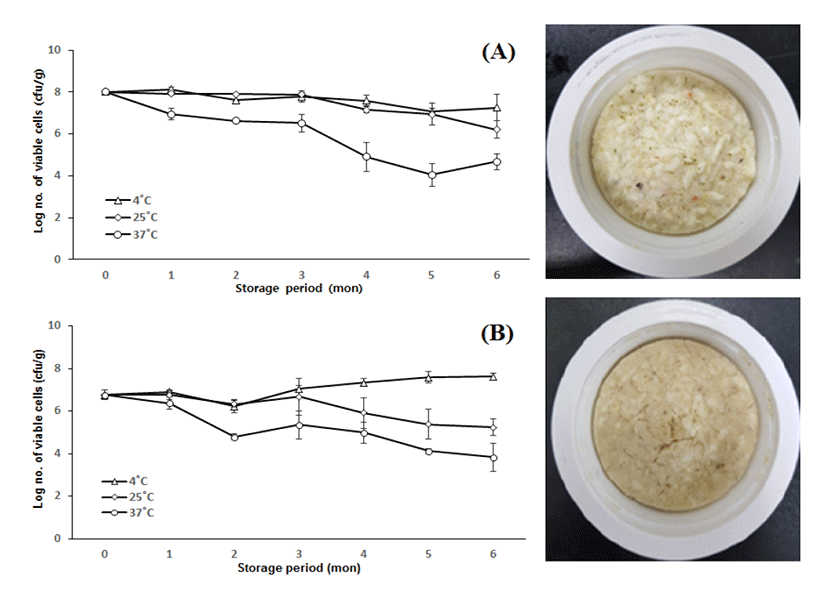
캡슐화한 균주를 첨가한 동결건조 죽제품의 저장 온도별(4℃, 25℃ 및 37℃) 생존율을 1개월 간격으로 6개월 동안 확인한 결과, 37℃에서 저장된 모든 제품은 저장 기간이 경과됨에 따라 생존 균수가 점차 감소하는 경향을 나타났다(Fig. 3). 반면, 4℃와 25℃에서 저장한 제품들은 대부분 초기 균수에 비해 큰 변화가 나타나지 않았으며, 초기 균수를 108 CFU/g 이상 첨가한 한우야채죽의 경우, 유산균 첨가 제품의 최종 목표인 107 CFU/g 이상의 균수를 보유하는 것을 알 수 있었다. 게살새우브로콜리 제품의 경우도, 개개 포장용기에 따라 다소 차이를 보이지만 4℃와 25℃에서 저장할 경우 37℃에 비해 큰 감소폭을 보이지 않았다. 이러한 결과는 본 연구에서 개발된 캡슐화 기술이 제품 가공 및 적용시에도 프로바이오틱스의 생존율을 증가시킬 수 있음을 알 수 있었다.
결론적으로 본 실험에서 사용된 저온 캡슐화 공법은 식품가공 공정 및 저장기간 그리고 다양한 환경 속에서도 프로바이오틱스의 생존율을 향상시킬 수 있는 보호 능력을 부여할 것이라 판단된다. 무엇보다 시제품의 저장 기간 중 균주의 생존율에 유의적인 영향을 미칠 수 있어 본 연구에 사용된 균주의 구강 건강 케어에 대한 활용도를 높일 수 있을 것이라 판단된다.
Fig. 1.
Scanning electron microscopy (A) and transmission electron microscopy (B) of encapsulated Weissella cibaria CMU.
Download Original Figure
Fig. 2.
Viability of encapsulated Weissella cibaria CMU after exposure to acid (A), bile (B) and heat (C) conditions for various durations. Data are expressed as the mean±SD of three experiments. *Significantly different values between control and encapsulation (p<0.05).
Download Original Figure
Fig. 3.
Viability of encapsulated Weissella cibaria CMU during storage at various temperatures (4℃, 25℃ and 37℃). (A), Beef and vegetable rice porridge; (B), Crabmeat, shrimp and broccoli rice porridge.
Download Original Figure
감사의 글
본 연구는 중소기업 기술혁신개발사업에 의해 지원되어 수행되었으며, 이에 감사드립니다(S2423435).
References
Adhikari, K., Mustapha, A. and Grun, I. U. 2003. Survival and metabolic activity of microencapsulated Bifidobacterium longum in stirred yogurt. J. Food Sci. 68:275-280 .


Ann, E. Y., Kim, Y. H., Oh, S. J., Imm, J, Y., Park, D. J., Han, K. S. and Sae, H. 2007. Microencapsulation of Lactobacillus acidophilus ATCC 43121 with prebiotic substrates using a hybridisation system. Int. J. Food Sci. Technol. 42:411-419 .


Ansari, F., Pourjafar, H., Jodat, V., Sahebi, J. and Ataei, A. 2017. Effect of eudragit S100 nanoparticles and alginate chitosan encapsulation on the viability of Lactobacillus acidophilus and Lactobacillus rhamnosus. AMB Express. doi: 10.1186/s13568-017- 0442-x .

Bae, E. K. and Kim, G. H. 2008. Encapsulation of avocado oil using spray drying. Korean J. Food Sci. Technol. 40:303-310 .

Choi, E. S., Lyu, J. Y. and Kim, H. Y. 2015. Association between oral health status and health related quality of life (EuroQoL-5 Dimension). J. Den. Hyg. Sci. 15:480-487 .


Chun, J. U. and Lee, K. H. 2017. The correlation between oral health factors and mental health factors in Korean adolescents. J. Korean Soc. Dent. Hyg. 17:669-680 .

Do, K. H., Park, H. E., Kang, M. S., Kim, J. T., Yeu, J. E. and Lee, W. K. 2018. Oral malodor-reducing effects by oral feeding of Weissella cibaria CMU in beagle dogs. Korean J. Vet. Res. 55:87-94 .

Health Insurance Review and Assessment Service. 2016. National health insurance statistical yearbook. Wonju, Korea .

Jang, H. J., Kang, M. S., Yi, S. H., Hong, J. Y. and Hong, S. P. 2016. Comparative study on the characteristics of Weissella cibaria CMU and probiotic strains for oral care. Molecules. doi: 10.3390/molecules21121752 .


Jung, C. M., Lee, M. K., Lee, H. A. and Park, J. Y. 2009. Low-temperature microencapsulation of sesame oil using fluidized bed granulation. Korean J. Food Sci. Technol. 41:27-31 .

Kang, M. S., Yeu, J. E., Oh, J. S., Shin, B. A. and Kim, J. H. 2017. Complete genome sequences of Weissella cibaria Strains CMU, CMS1, CMS2, and CMS3 isolated from infant saliva in South Korea. Genome Announc. doi: 10.1128/genomeA.01103-17 .


Kim, D. M, Hong, W. K., Kong, S. S. and Lee, U. Y. 2013. Novel encapsulation with new glyceryl ester vesicle enhances stability of nanoemulsion containing astaxanthin. J. Soc. Cosmet. Scientists Korea. 39:225-231 .


Kim, J. Y. and You, S. S. 2017. Development of a commercial process for micro-encapsulation of lactic acid bacteria using sodium alginate. Korean Chem. Eng. Res. 55:313-321 .

Kim, Y. R. 2017. Comparison of oral health behavior and oral health indexes between patients undergoing scaling regularly and those undergoing scaling irregularly. Korean J. Health Management 11:170-180 .


Minekus, M., Alminger, M., Alvito, P., Ballance, S., Bohn, T., Bourlieu, C., Carriere, F., Boutrou, R., Corredig, M., Dupont, D., Dufour, C., Egger, L., Golding, M., Karakaya, S., Kirkhus, B., Le Feunteun, S., Lesmes, U., Macierzanka, A., Mackie, A., Marze, S., McClements, D. J., Menard, O., Recio, I., Santos, C. N., Singh, R. P., Vegarud, G. E., Wickham, M. S., Weitschies, W. and Brodkorb, A. 2014. A standardised static in vitro digestion method suitable for food an international consensus. Food Funct. 5:1113- 1124 .



Muthukumarasamy, P., Allan-Wojtas, P. and Holley, R. A. 2006. Stability of Lactobacillus reuteri in different types of microcapsules. J. Food Sci. 71:20-24 .


Nag, A., Han, K. S. and Singh, H. 2011. Microencapsulation of probiotic bacteria using pH-induced gelation of sodium caseinate and gellan gum. Int. Dairy J. 21:247-253 .


Park, J. H., Ahn, S. H., Gu, H. J., Choi, Y. H. and Song, K. B. 2010. Inhibitory effects on colonization of Streptococcus mutans by eighteen months xylitol consumption. J. Korea Acad. Ind. Coop. Soc. 11:375-382 .


SAS. 2008 SAS/STAT software for PC. Release 9.2, SAS InstituteInc., Cary, NC, USA .

Yoon, S. U., Nam, I. S. and Jun, M. S. 2014. The relationship between mental illness state and oral health management of mental patients in mental health care institutions. J. Korean Soc. Dent. Hyg. 14:547-553 .