서 론
바이오제닉 아민(Biogenic amine, BA)은 아미노산의 탈탄산작용 또는 알데하이드와 케톤의 아미노화와 아미노기 전이반응에 의해 주로 생성되는 질소화합물(Halasz, 1994)로, 아민그룹의 개수에 따라 모노아민류(monoamnin), 다이아민류(diamine) 및 폴리아민류(polyamine)로 분류한다. 화학적 구조에 의해서는 지방족 화합물인 petrescine, cadaverine, spermine, spermidine과 방향족 화합물인 histamine, trypramine으로 나눌 수 있다. Gerner와 Meyskens(2004)에 따르면 바이오제닉 아민은 세포 내에서 세포증식, 분화 및 성장에 중요한 역할을 수행한다고 보고하였고, Igarashi 등(2001)은 체내에서 직간접적으로 신경전달 물질로서 작용하고, 혈압조절 및 혈류 등의 심혈관계에도 영향을 미친다고 보고하였다.
식품으로 섭취된 바이오제닉 아민은 체내 효소적 대사과정을 거처 독성물질이 해독되는 것으로 알려져 있어 일반적으로 크게 문제가 되지 않으나, 과량의 바이오제닉 아민을 섭취할 경우나 유전적으로 바이오제닉 아민을 대사하는 효소의 생산에 문제가 있을 경우, 인체 심각한 경향을 준다고 보고되고 있다. 또한 phenelzine은 우울증 치료제로, 이를 복용하는 사람이 바이오제닉 아민을 소량 섭취할 경우에도 건강상의 심각한 문제를 야기하게 된다(Bodmer et al., 1999; Caston et al., 2002; Lee et al., 2012).
자연치즈는 중 숙성치즈는 어류 다음으로 Histamine 중독이 많이 발생되며, 주요 생성 아민류는 histamine, tyramine, cadaverine, putrescine, trytamine, phenylethylamine 등이 있으며, 특히 tyramine은 치즈반응(cheese reaction)이라고 불리어지는 원인 물질로 혈관을 수축하여 고혈압을 유발한다고 보고하고 있다(Youdim, 1995). 유럽 등의 치즈 제조 선진국은 바이오제닉 아민의 함량을 저감화 하기 위한 연구가 활발히 진행되고 있으나, 국내 치즈산업에서는 바이오제닉 아민에 대한 연구는 미흡한 실정이다. 국내 바이오제닉 아민에 대한 연구로는 주로 전통발효식품에 대한 바이오제닉 아민 분석 및 저감화에 대한 연구가 주로 이뤄지고 있어(Halasz, 1994; Mah et al., 2008; Naila et al., 2010), 자연치즈 중 숙성치즈에 대한 바이오제닉 함량에 대한 연구가 필요한 실정이다.
따라서 본 연구는 국내산 숙성치즈의 바이오제닉 아민 함량 분석을 위한 기초연구로 HPLC 분석법을 이용한 숙성치즈의 바이오제닉 함량 분석법을 검토하였다.
재료 및 방법
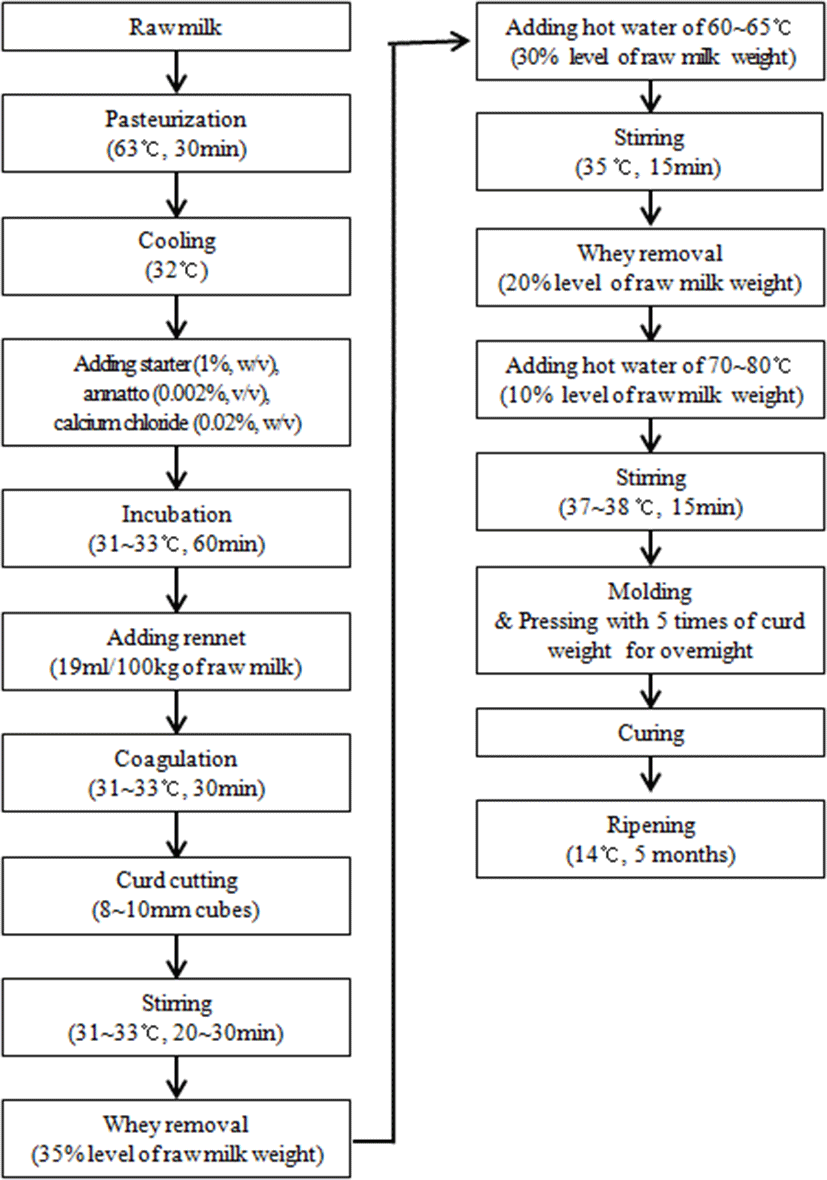
본 연구에 사용된 고다치즈는 Flora Danica 50(Chr. Hansen, Denmark)을 starter로 사용하여 제조하였으며, 이때의 구성 균주는 Lactococcus lactis subsp. cremoris, Lactococcus lactis subsp. diacetylactis, Lactococcus lactis subsp. lactis, Leuconostoc mesenteroides subsp. cremoris로 구성되어 있다. 자세한 제조 방법은 Fig. 1에 나타내었다.
바이오제닉 아민 표준품은 Sigma사(St. Louis, MO, USA)의 Histamine dihydrochloride(99%), Tyramine hydrochloride(98%), β-Phenylethylamine hydrochloride(98%), Putrescine dihydrochloride(98%), Cadaverine(95%), Spermidine(99%), Tryptamine hydrochloride(99%), Ethanolamine hydrochloride(99%) 및 Butylamine(99.5%)을 구입하여 사용하였다. 각각의 바이오제닉 아민 표준품은 0.1 N HCl에 녹여 약 1,000 mg/L가 되도록 한 것을 표준용액으로 하였다.
바이오제닉 아민 표준용액은 0.1 N HCl을 이용하여 적당히 희석하여 농도별 표준액을 제조한 다음, 피크 면적 비를 구하여 검량선을 작성하였고, 작성된 검량선으로부터 직선식의 상관계수(기준: R2=0.99 이상)를 구하여 직선성을 검토하였다.
검량선의 직선성 범위가 좋은 부분을 이용하여 다음과 같은 식을 이용하여 검출한계(LOD), 정량한계(LOQ)를 산출하였다.
검출한계 = 3.3×σ/S (S/N=3)
정량한계 = 10×σ/S (S/N=10)
이때 σ는 절편의 평균표준편차이며, S는 기울기의 평균을 의미한다.
바이오제닉 아민 분석을 위한 시료 전처리는 Garcia-Garcia 등(2009)의 방법과 일본위생시험법의 불휘발성 부패아민 분석법 및 Lee 등(2009)의 방법을 변형하여 사용하였다. 즉, 검체 5 g을 정확히 취하여 15 mL의 0.1 N HCl을 가하여 균질화하고, 이것을 원심분리(4,000× g, 15 min)한 다음 상층액을 위하여 3회 반복하여 얻은 상층액을 합치고, 0.1 N 염산을 가해 50 mL로 한 것을 시험용액으로 하였다. 이 용액 1 mL를 취하여 0.5 mL의 포화 Na2CO3, 1 mL의 1% dansyl chloride acetone solution를 가하여 45℃에서 1시간동안 유도체화를 시킨 다음, 1 mL의 10% proline 용액을 첨가하여 과량의 유도체화 시약을 제거하였다. 여과액에 5 mL의 ether를 가하여 3분간 진탕한 후 상층액을 취하여 질소가스를 이용하여 건조시키고, acetonitrile 2 mL를 가한 후, 0.45 μm syringe filter로 여과한 샘플을 HPLC (e2695, Waters Co., USA)로 분석하였다.
바이오제닉 아민 분석을 HPLC(e2695, Waters Co., USA)을 이용하여 분석하였고, 조건은 다음과 같다. 분석용 분석용 칼럼은 CapcellPak C18 Column(4.6×250 mm, 5 mm, Shiseido Co., Tokyo, Japan)을 사용하였으며, UV 254 nm에서 검출하였다. HPLC 측정조건은 컬럼 온도를 40℃에서 이동상의 유속을 1 mL/min에서 조정하였으며, 주입량은 10 μL로, 이동상은 A는 0.1% glacial acetic acid in water, B는 0.1% glacial acetic acid in acetonitrile로 하였고, 이동상 B의 농도구배는 55%로 10분, 65%로 5분, 80%로 10분, 90%로 15분으로 총 40분간 시행하였다.
결과 및 고찰
바이오제닉 아민인 Histamine dihydrochloride, Tyramine hydrochloride, β-Phenylethylamine hydrochloride, Putrescine dihydrochloride, Cadaverine, Spermidine, Tryptamine hydrochloride, Ethanolamine hydrochloride 및 Butylamine 9종은 표준용액 1,000 ppm으로 조정한 다음, 각각의 농도는 10, 25, 50 및 75 ppm 농도로 제조하여 HPLC로 분석하였다. 이때 얻은 피크 면적을 Y축으로, 표준액 농도를 X축으로 하여 검량선을 작성하여 나타내었다(Fig. 2). 이때 검량선 식은 Histamine dihydrochloride는 Y = 2,724x × 농도 + 829.1 (r =0.998), Tyramine hydrochloride는 Y = 6,760x × 농도 – 1,710 (r = 0.999), β-phenylethylamine hydrochloride는 Y = 5,494x × 농도 + 462.5 (r = 0.999), Putrescine dihydrochloride는 Y = 6,539x × 농도 + 1,919 (r = 0.998), Cadaverine는 Y = 4,949x × 농도 + 4,828 (r = 0.999), Spermidine는 Y = 4,570x × 농도 + 3,961 (r = 0.999), Tryptamine hydrochloride는 Y = 4,386x × 농도 + 1,082 (r = 0.999), Ethanolamine hydrochloride는 Y = 3,947x × 농도 + 828 (r = 0.998) 및 Butylamine는 Y = 4,049x × 농도 – 2,038 (r = 0.999)로 나타나 모두 양호한 수준이었다.
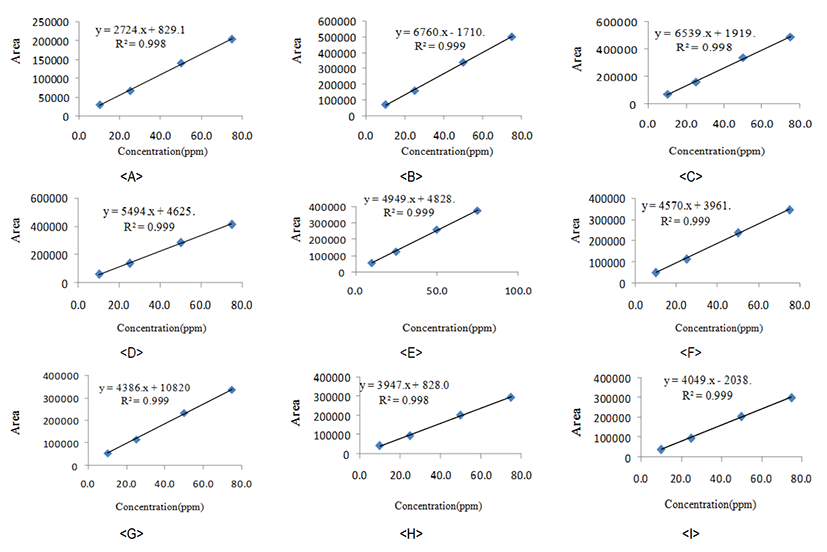
가장 직선성이 좋은 부분을 이용하여 Histamine dihydrochloride, Tyramine hydrochloride, β-phenylethylamine hydrochloride, Putrescine dihydrochloride, Cadaverine, Spermidine, Tryptamine hydrochloride, Ethanolamine hydrochloride 및 Butylamine 의 검출한계와 정량한계를 구하여 Table 1에 나타내었다. 즉, Histamine dihydrochloride의 검출한계 및 정량 한계는 각각 3.7 및 11.3 ppm, Tyramine hydrochloride는 각각 3.4 및 10.4 ppm, β- Phenylethylamine hydrochloride는 각각 3.4 및 10.3 ppm, Putrescine dihydrochloride는 각각 4.0 및 12.2 ppm, Cadaverine는 각각 3.4 및 10.4 ppm, Spermidine는 각각 3.4 및 10.5 ppm, Tryptamine hydrochloride는 각각 3.5 및 10.7 ppm, Ethanolamine hydrochloride는 각각 4.1 및 12.5 ppm 및 Butylamine는 각각 3.4 및 10.4 ppm으로 나타났다.
바이오제닉 아민의 HPLC 분석을 위하여 각각의 바이오제닉 아민을 고다치즈에 spiking하여 최종 농도를 40 ppm으로 조정하였고, 이를 HPLC로 분석한 결과는 Table 2에 나타내었다. Histamine dihydrochloride는 112%, Tyramine hydrochloride는 104%, β-Phenylethylamine hydrochloride는 93%, Putrescine dihydrochloride는 108%, Cadaverine는 91%, Spermidine는 102%, Tryptamine hydrochloride는 90%, Ethanolamine hydrochloride는 101% 및 Butylamine는 92%으로 나타났다.
결론적으로 바이오제닉 아민 9종에 대한 직선성, 검출한계, 정량한계 및 회수율을 측정한 결과, 모두 만족스러운 결과를 나타냈으며, 숙성치즈의 바이오제닉 아민에 대한 기초자료로 사용될 수 있을 것으로 기대된다.
요 약
본 연구는 국내산 숙성치즈의 바이오제닉 아민 함량 분석을 위한 기초연구로 HPLC 분석법을 이용한 숙성치즈의 바이오제닉 아민 함량 분석법을 검토하였다.
본 연구에서 사용된 바이오제닉 아민의 종류는 Histamine dihydrochloride, Tyramine hydrochloride, β-Phenylethylamine hydrochloride, Putrescine dihydrochloride, Cadaverine, Spermidine, Tryptamine hydrochloride, Ethanolamine hydrochloride 및 Butylamine로 총 9종이었으며, 분석항목은 직선성, 검출한계, 정량한계 및 회수율을 측정하였다. 각각의 바이오제닉 아민의 직선성은 모두 r = 0.99 이상으로 측정되어 양호하게 분석되었고, 검출한계는 각각 3.7, 3.4, 3.4, 4.0, 3.4, 3.4, 3.5, 4.1 및 3.4 ppm, 정량한계는 11.3, 10.4, 10.3, 12.2, 10.4, 10.5, 10.7, 12.5 및 10.4 ppm으로 나타났으며, 회수율은 112, 104, 93, 108, 91, 102, 101 및 92%로 나타났다. 따라서 본 연구를 통하여 바이오제닉 아민 9종에 대한 직선성, 검출한계, 정량한계 및 회수율을 측정한 결과, 모두 만족스러운 결과를 나타냈으며, 숙성치즈의 바이오제닉 아민에 대한 기초자료로 사용될 수 있을 것으로 기대된다.