ARTICLE
케이신 포스포펩티드/키토올리고당 나노 복합체의 유식품 적용 연구
Application of Casein Phosphopeptide/Chitosan Oligosaccharide Nanocomplex to Dairy Foods
Ho-Kyung Ha
1,†
, Yun-Seo Baek
2,†
, Won-Jae Lee
2,*
1Dept. of Animal Science and Technology, Sunchon National University, Sunchon, Korea
2Dept. of Animal Bioscience and Institute of Agriculture and Life Science, Gyeongsang National University, Jinju 52828, Korea
*Corresponding author : Won-Jae Lee, Dept. of Animal Bioscience and Institute of Agriculture and Life Science Gyeongsang National University, Jinju, Korea, Tel : +82-55-772-1884, Fax : +82-55-772-1889, E-mail :
wjleewisc@gnu.ac.kr
†These authors contributed equally to this study.
© Copyright 2021, Korean Society of Dairy Science and Biotechnology. This is an Open Access article distributed under the terms of the
Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0/) which permits
unrestricted non-commercial use, distribution, and reproduction in any
medium, provided the original work is properly cited.
Received: Mar 19, 2021; Revised: Mar 25, 2021; Accepted: Mar 25, 2021
Published Online: Mar 31, 2021
Abstract
The aim of this research was to investigate the potential application of casein phosphopeptide (CPP)/chitosan oligosaccharide (CSO) nanocomplexes to dairy foods. The physical stability of CPP/CSO nanocomplexes during storage in model dairy foods including milk and yogurt was assessed by measuring the size and polydispersity index of the nanocomplexes. Encapsulation efficiency and in vitro vitamin D release from CPP/CSO nanocomplexes during gastrointestinal digestion were determined using HPLC. CPP/CSO nanocomplexes with increased CPP concentrations and decreased pH displayed significantly increased average particle size. During storage in model dairy foods, CPP/CSO nanocomplexes prepared with lower CPP concentrations and raised pH exhibited excellent physical stability. Vitamin D encapsulation efficiency increased significantly (p<0.05) as CPP concentration and/or pH decreased. Less than 3% vitamin D were released under gastric digestion conditions in vitro, while 91% of encapsulated vitamin D was released by 2 h of incubation under intestinal conditions, indicating that CPP/CSO nanocomplexes could effectively protect vitamin D from gastric conditions for delivery to the intestines. In conclusion, CPP/CSO nanocomplexes can be applied to dairy foods as an effective vitamin D delivery system.
Keywords: casein phosphopeptide; chitosan oligosaccharide; nanocomplex; dairy food application; in vitro release
서 론
우리나라는 2017년 이미 고령사회에 진입하였고, 2025년에는 전체 인구대비 노인인구 구성비가 20%가 넘어서는 초고령사회에 진입할 것으로 예상되고 있다[1]. 특히, 보건복지부 통계에 따르면 우리나라 만 65세 이상 성인의 칼슘 섭취량은 권장섭취량 대비 82% 수준이다. 본 연구진의 기존 연구에서는 칼슘 흡수를 증진시키기 위한 전달체로서 food-grade biopolymer인 카제인포스포펩티드(casein phosphopeptide, CPP)와 키토올리고당(chitosan oligosaccharide, CSO)을 이용하여 약 187–280 nm 크기를 지니는 나노 복합체를 성공적으로 제조하였다[2]. 그러나 CPP/CSO 나노 복합체를 포함한 food-grade 나노 전달체의 유식품 적용성 및 생리활성 물질의 위장관 내 전달 특성에 관한 연구는 매우 부족한 실정이다.
본 연구에서는 체내 칼슘 흡수 증진을 극대화하기 위해 기존에 칼슘 흡수 증진효과가 있다고 알려진 CPP[3,4]와 CSO[5]를 사용하여 제조한 나노 복합체 내에 비타민 D를 포집하고자 하였다. 지용성 생리활성물질인 비타민 D는 체내 칼슘흡수를 조절하고, 뼈 건강 증진 및 골다공증 예방에 효과가 있는 호르몬으로 대부분은 자외선 노출에 의해 피부에서 합성되지만, 현대인의 부족한 비타민 D 합성으로 인해 음식 또는 보충제 형태로 비타민 D를 섭취하고 있다[6,7]. 그러나 비타민 D를 포함한 생리활성물질은 유식품공정(제조 및 저장)과 위장관 내에서 빛, 산소, 열 등에 노출되어 쉽게 활성이 소실된다[8]. 따라서 비타민 D를 효과적으로 포집하여 장 내로 안전하게 전달할 수 있는 Food-grade 나노 전달체 개발이 필요한 실정이다. 따라서 본 연구의 목적은 주요 제조 공정 요인인 CPP 농도 및 pH를 조절하여 제조한 CPP/CSO의 나노복합체의 유식품 적용 후 저장 기간 동안의 물리적 안정성을 평가하고, 제조공정 요인인 CPP 농도와 pH에 따른 나노 복합체 내 비타민 D의 포집 효율을 측정하며, 포집된 비타민 D의 위장관 내 in vitro release를 평가하는 것이다.
재료 및 방법
1. 시약
CPP는 FrieslandCampina(Netherlands)에서, CSO은 Amicogen(Korea)에서 제공받아 사용하였다. 비타민 D3(cholecalciferol)는 Sigma-Aldrich(USA)에서 구입하였다.
2. 나노 복합체의 유식품 적용성 연구
CPP/CSO 나노 복합체는 본 연구팀의 기존 연구 방법인 modified ionic gelation 방법[2]에 따라 제조하였다. 나노 복합체의 유식품 적용성 평가를 위해 CPP의 최종 농도는 0.1, 0.2, 또는 0.3%(w/v)로, pH는 5.5 또는 6.5로 조절하여 나노 복합체를 제조한 후 동결건조기(FD-1000, Tokyo Rikakikai, Japan)를 이용하여 동결건조하였다. 그런 다음 분말 형태의 나노 복합체를 1 mg/mL 농도로 model milk(pH 6.7) 또는 model yogurt(pH 4.6)에 분산시킨 후 4°C에서 12일간 저장하면서 나노 복합체의 입자크기(particle size)와 다분산지수(polydispersity index)를 입도분석기(particle size analyzer(Zetasizer Nano-ZS, Malvern, UK)로 측정하여 유식품 내 물리적 안정성을 평가하였다[9].
3. 나노 복합체의 비타민 D 포집 효율 평가
CPP/CSO 나노 복합체의 칼슘 전달 극대화를 위한 비타민 D의 포집 효율은 high performance liquid chromatography(HPLC, 1290 Infinity II LC, Agilent Technologies, USA)를 이용하여 평가하였다[10]. 포집 효율(encapsulation efficiency, EE) 평가를 위해 비타민 D3 함유 CPP/CSO 나노 복합체를 10,000 g에서 30분간 원심분리하여 상층액의 포집되지 않은 비타민 D3를 회수한 후 nylon syringe filter로 여과한 후 20 uL를 reverse phase C18 Column(3.5 μm, 150×4.6 mm)에 주입하였다. 이동상(mobile phase)은 acetonitrile/methanol 혼합액(90:10)을 사용하였으며, 유속(flow rate)은 1.0 mL/min, 검출 파장(detection wavelength)은 265 nm로 설정하였다. CPP/CSO 나노 복합체 내 비타민 D3의 포집 효율은 아래의 식에 따라 계산하였다[11].
4. 비타민 D의 in vitro release 평가
CPP/CSO 나노 복합체에 포집된 비타민 D의 위장관 내 조건에서의 release는 Chávarri[12]와 García-Sartal et al.[13]의 in vitro digestion 방법을 사용하여 평가하였다. 위(stomach)와 소장(small intestine)에서의 release 평가를 위해 simulated gastric juice(SGJ)와 simulated intestinal juice(SIJ)를 준비하였다. SGJ는 증류수에 0.9%(w/v) NaCl과 0.3%(w/v) pepsin을 용해시킨 후 pH를 2.0으로 조절하여 준비하였고, SIJ는 증류수의 pH를 7.5로 조절하여 준비하였으며, SGJ와 SIJ 모두 0.45 μm syringe filter(Polyethersulfone, HYUNDAI Micro., Korea)로 여과한 다음 나노 복합체와 9:1 비율로 혼합하였다. 그런 다음 SGJ/나노 복합체 혼합물과 SIJ/나노 복합체 혼합물을 37°C에서 30분과 120분 동안 각각 배양하면서 release 되는 비타민 D의 양을 HPLC를 이용하여 평가하였다.
5. 통계 분석
제조 공정 요인(CPP 농도 및 pH) 및 저장 기간에 따른 CPP/CSO 나노 복합체의 유식품 적용 안정성과 비타민 D의 포집효율 및 in vitro release는 SAS software package(Version 9.1, SAS Institute, USA)를 사용하여 분석하였으며, 모든 실험은 3번 반복하여 평균±표준편차로 나타내었다. 나노 복합체의 제조공정과 저장 기간에 따른 물리적 안정성은 repeated measures analysis of variance(ANOVA)로 분석하였다. 또한 제조공정 요인에 따른 CPP/CSO 나노 복합체 내 비타민 D의 포집 효율 및 포집된 비타민 D의 in vitro release는 일원분산분석(one-way ANOVA)을 통해 분석하였다. 일원분산분석의 경사별 차이 유의성은 Fisher의 최소유의차(least significant difference, LSD) 법으로 5% 유의수준(p<0.05)에서 검정하였다.
결과 및 고찰
1. 나노 복합체의 유식품 적용성 연구
1) Model milk
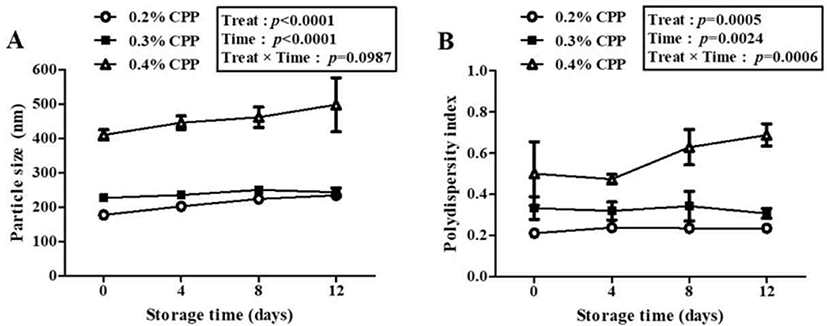
제조공정요인인 CPP 농도 및 pH에 따른 CPP/CSO 나노 복합체의 유식품 적용성은 동결건조된 나노 복합체를 model milk(Figs. 1 and 2)와 model yogurt(Figs. 3 and 4)에 적용 후 4°C에서 12일 저장 기간 동안 나노 복합체의 크기 및 다분산지수 측정을 통해 평가하였다. 우선 model milk에서 저장 기간동안 CPP 농도에 따른 나노 복합체의 크기를 repeated-measures ANOVA로 분석한 결과, CPP 농도(p<0.0001)와 저장 기간(p<0.0001)에는 유의적 차이가 있는 반면, CPP 농도와 저장 기간 간 상호작용(p=0.0987)에는 유의적 영향을 미치지 않았다(Fig. 1A). CPP 농도 0.2%, 0.3%, 0.4%(w/v)로 제조한 나노 복합체는 저장 0일차에 각각 178.0, 227.2, 410.6 nm에서 저장 12일차에 각각 234.6, 243.8, 498.6 nm로 크기가 최대 1.3배까지 증가하였다. Model milk에서 저장 기간 동안 CPP 농도에 따른 나노 복합체의 다분산지수는 CPP 농도(p=0.0005), 저장 기간(p= 0.0024) 및 이들 간 상호작용(p=0.0006) 모두 유의적인 영향을 받음을 알 수 있었다(Fig. 1B). 그 중 CPP 농도 0.2%(w/v)로 제조한 나노 복합체의 경우 12일간의 저장 기간 동안 다분산지수 0.3 이하의 균일한 입도[14]를 가졌다. 이를 통해 model milk 내에서 200 nm 초반의 작은 크기와 균일한 입도 분포를 나타내는 CPP 농도 0.2%(w/v)에서 제조한 나노 복합체가 가장 높은 유식품 적용성을 지니는 조건임을 알 수 있었다.
Fig. 1.
Effects of casein phosphopeptide (CPP) concentration level on the size (A) and polydispersity index value (B) of CPP/chitosan oligosaccharide (CSO) nano complexes during storages in model milk at 4°C for 12 days. CPP/CSO nano complexes were prepared with 0.2 (○), 0.3 (■), or 0.4% (△) (w/v) CPP solution and 0.003% (w/v) CSO solution at pH 6.5. The error bars on each point indicate the standard deviations of three replicates. Significant effects of CPP concentration level over time were determined by using repeated-measures ANOVA. Time, storage time in days; treat, CPP concentration level; time×treat, interaction between time and treat; ANOVA, analysis of variance.
Download Original Figure
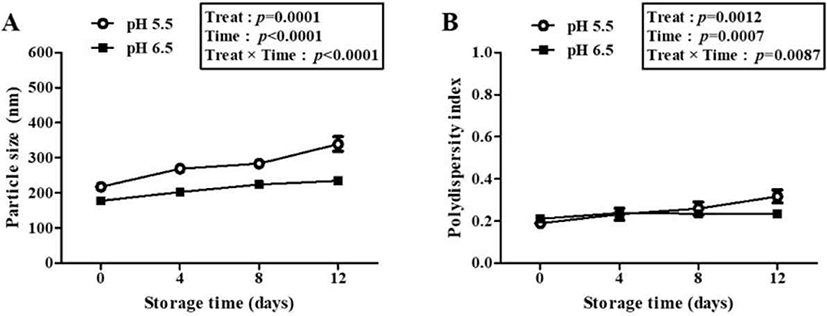
Fig. 2.
Effects of pH on the size (A) and polydispersity index value (B) of casein phosphopeptide (CPP)/chitosan oligosaccharide (CSO) nano complexes during storages in model milk at 4°C for 12 days. CPP/CSO nano complexes were prepared with 0.2% (w/v) CPP solution and 0.003% (w/v) CSO solution at pH 5.5 (○) or 6.5 (■). The error bars on each point indicate the standard deviations of three replicates. Significant effects of CPP concentration level over time were determined by using repeated-measures ANOVA. Time, storage time in days; treat, CPP concentration level; time×treat, interaction between time and treat; ANOVA, analysis of variance.
Download Original Figure
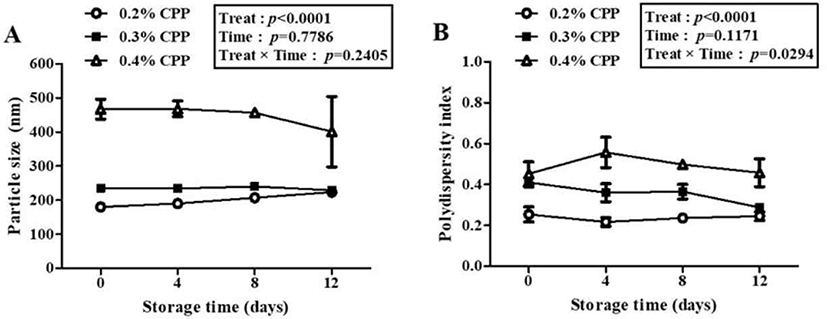
Fig. 3.
Impacts of casein phosphopeptide (CPP) concentration level on the size (A) and polydispersity index value (B) of CPP/chitosan oligosaccharide (CSO) nano complexes during storages in model yogurt at 4°C for 12 days. CPP/CSO nano complexes were prepared with 0.2 (○), 0.3 (■), or 0.4% (△) (w/v) CPP solution and 0.003% (w/v) CSO solution at pH 6.5. The error bars on each point indicate the standard deviations of three replicates. Significant effects of CPP concentration level over time were determined by using repeated-measures ANOVA. Time, storage time in days; treat, CPP concentration level; time×treat, interaction between time and treat; ANOVA, analysis of variance.
Download Original Figure
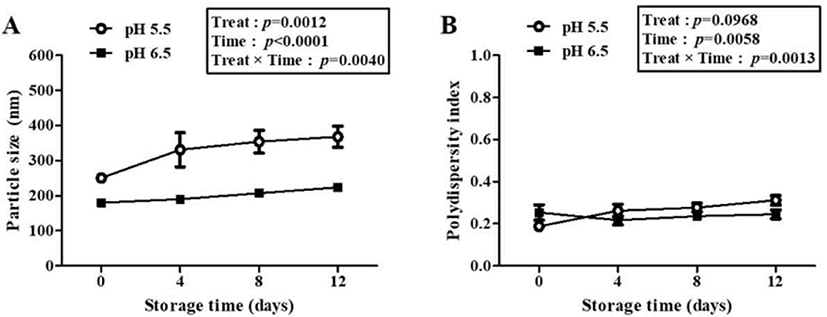
Fig. 4.
Impacts of pH on the size (A) and polydispersity index value (B) of casein phosphopeptide (CPP)/chitosan oligosaccharide (CSO) nano complexes during storages in model yogurt at 4°C for 12 days. CPP/CSO nano complexes were prepared with 0.2% (w/v) CPP solution and 0.003% (w/v) CSO solution at pH 5.5 (○) or 6.5 (■). The error bars on each point indicate the standard deviations of three replicates. Significant effects of CPP concentration level over time were determined by using repeated-measures ANOVA. Time, storage time in days; treat, CPP concentration level; time×treat, interaction between time and treat; ANOVA, analysis of variance.
Download Original Figure
또, 다른 주요 제조 공정요인인 pH에 따른 나노 복합체의 model milk 내 적용성 평가 결과는 Fig. 2에 제시되었다. 그 결과, pH(p=0.0001), 저장 기간(p<0.0001) 및 이들 간 상호작용(p< 0.0001) 모두 입자 크기에 유의적인 영향을 미치는 것을 알 수 있었다. pH 5.5와 6.5에서 제조된 나노 복합체는 저장 0일차에 각각 178.0 및 217.6 nm에서 저장 기간이 증가함에 따라 점차 증가하여 저장 12일차에 각각 234.6 및 339.4 nm 크기를 가졌다. pH 및 저장 기간에 따른 다분산지수 측정 결과, pH(p=0.0012), 저장 기간(p=0.0007) 및 이들 간 상호작용(p=0.0087) 모두 다분산지수에 유의적인 영향을 미쳤다. 특히 pH 5.5에서 제조된 나노 복합체의 경우 저장 12일차에는 0.317의 다분산지수를 나타낸 반면, pH 6.5에서 제조된 나노 복합체는 저장 12일차에도 다분산지수 0.236으로 균일한 입도 분포를 나타내고 있음을 확인하였다. 결과적으로 model milk에서 가장 높은 안정성을 지닌 나노 복합체 제조 공정 조건은 CPP 농도는 0.2%(w/v), pH는 6.5임을 알 수 있었다.
2) Model yogurt
Fig. 3은 CPP 농도 및 저장 기간에 따른 model yogurt 내 CPP/CSO 나노 복합체의 입자크기와 다분산지수를 나타낸다. 입자 크기의 경우, CPP 농도는 유의적인 영향(p<0.0001)을 미치는 반면, 저장 기간(p=0.7786) 및 CPP 농도와 저장 기간 간 상호작용(p=0.2405)은 유의적인 영향을 미치지 않음을 알 수 있었다(Fig. 3A). 또한 다분산지수의 경우, CPP 농도(p<0.0001) 및 CPP 농도와 저장 기간 간 상호작용(p=0.0294)은 유의적인 영향을 미치는 반면, 저장 기간(p=0.1171)은 유의적인 영향을 미치지 않았다(Fig. 3B). 특히 CPP 농도 0.2%(w/v)에서 제조된 나노 복합체의 경우, model yogurt에서 12일간 저장 후에도 200 nm 초반대의 작은 크기와 다분산지수 0.3 이하의 균일한 입도 분포를 유지하고 있어 가장 높은 유식품 적용성을 지닌 제조 공정 조건임을 확인하였다.
pH 및 저장 기간에 따른 model yogurt 내 CPP/CSO 나노 복합체의 입자 크기와 다분산지수는 Fig. 4에 나타내었다. Repeated-measures ANOVA로 분석한 결과, pH(p=0.0012), 저장 기간(p<0.0001) 및 이들 간 상호작용(p=0.0040)은 모두 입자 크기에 유의적인 영향을 미쳤다(Fig. 4A). pH 5.5에서 제조된 나노 복합체의 경우 저장 0일차에 251.0에서 저장 12일차에 368.2 nm로 크기가 약 1.5배로 크게 증가한 반면, pH 6.5에서 제조된 나노 복합체는 저장 0일차에 180.4에서 저장 12일차에 223.9 nm로 약 1.2배로 소폭 증가하였다(Fig. 4A). 다분산지수의 경우, pH(p=0.0968)는 유의적인 영향을 미치지 않았으나, 저장 기간(p=0.0058) 및 pH와 저장 기간의 상호작용(p=0.0013) 경우 유의적인 영향을 나타냈다. 특히, pH 5.5에서 제조된 나노 복합체는 저장 12일차에 다분산지수가 0.3 이상(0.312)으로 증가한 반면 pH 6.5에서 제조된 나노 복합체는 저장 12일차 이후에도 0.3이하(0.245)의 다분산지수로 균일한 입도 분포를 유지하는 것을 확인하였다(Fig. 4B).
결과적으로 model milk뿐만 아니라, model yogurt에서도 가장 작은 입자 크기와 균일한 입도 분포를 유지하고 있는 CPP 0.2%(w/v) 및 pH 6.5가 유식품 적용시 높은 안정성을 유지할 수 있는 나노 복합체를 제조할 수 있는 최적 제조 공정요인임을 알 수 있었다.
2. 나노 복합체 내 비타민 D 포집 효율 평가
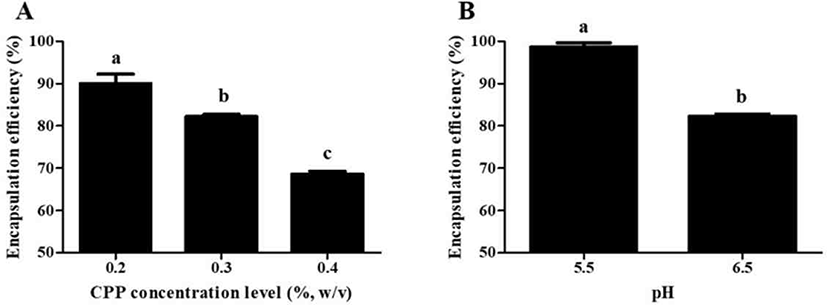
Biopolymer 전달체를 이용한 생리활성물질의 포집시 사용되는 biopolymer의 구조, 작용기, 전하뿐만 아니라, pH 및 biopolymer의 비율 등과 같은 제조 공정요인이 큰 영향을 미친다고 알려져 있다[15]. 본 연구에서 제조 공정요인으로 사용된 CPP 농도 및 pH에 따른 CPP/CSO 나노 복합체의 비타민 D 포집 효율 결과는 Fig. 5에 제시되었다. 그 결과, CPP 농도가 0.4에서 0.2%(w/v)로 감소함에 따라 비타민 D 포집 효율이 약 68.7%에서 90.0%로 유의적으로(p<0.05) 증가하였다(Fig. 5A). pH 6.5에서 제조된 CPP 나노 복합체는 약 –19.0 mV에서 –25.7 mV의 제타전위를 지니고 있고, CPP 농도가 0.2%에서 0.4%(w/v)로 증가함에 따라 음전하가 증가하였다[2]. 즉, CPP 농도 증가는 양전하를 지니는 CSO 대비 음전하를 지니는 CPP의 비율을 증가시키게 되고, 이에 따라 CSO와 CPP 간 정전기적 상호작용 극대화로 인해 전하의 불균형을 초래하게 되어 결과적으로 높은 CPP 농도에서 낮은 비타민 포집 효율을 보인 것으로 사료된다[16]. 단백질(gelatin)과 다당류(cress seed m mucilage)를 이용하여 비타민 D를 포집한 Jannasari et al.[16]의 연구에서도 다당류 대비 단백질 비율 증가는 전하의 불균형을 초래하여 비타민 D의 포집 효율을 감소시킨다고 보고하였다.
Fig. 5.
Effects of casein phosphoppeptide (CPP) concentration level (A) and pH (B) on the encapsulation efficiency of vitamin D in CPP and chitosan oligosaccharide (CSO) nano complexes. CPP/CSO nano complexes were prepared with 0.2, 0.3, or 0.4% (w/v) CPP solution and 0.003% (w/v) CSO solution at pH 5.5 or 6.5. Different letters on a column indicate significant differences (p<0.05).
Download Original Figure
나노 복합체 제조 시 pH가 6.5에서 5.5로 감소함에 따라 비타민 D 포집 효율은 약 82.3%에서 98.7%로 유의적으로(p<0.05) 증가하였다(Fig. 5B). 기존의 다양한 전달체 연구에 있어 단백질(펩티드)와 다당류를 함께 사용할 경우, 포집된 생리활성물질의 diffusion을 감소시키는 barrier effect를 향상시켜 생리활성물질을 효과적으로 포집, 보호할 수 있다고 보고되었다[17,18]. 본 연구에서는 등전위점(isoelectric point, pI)이 3.1인 CPP와 pKa가 6.3인 CSO[2]를 사용하여 나노 복합체를 제조하였다. 따라서 제조 공정 요인인 pH가 6.5에서 5.5로 감소할 경우, CPP 표면의 음전하(negative charges)가 감소하여 CPP 분자간 electrostatic repulsion이 감소하고 CSO 표면의 양전하(positive charges)가 증가하게 되기 때문에 CPP와 CSO간 상호작용이 증가하게 되고 결과적으로 포집된 비타민 D의 diffusion을 감소시켜 더 많은 양의 비타민 D를 나노 복합체 내에 포집할 수 있게 된 것으로 사료된다.
3. 비타민 D의 in vitro release 평가
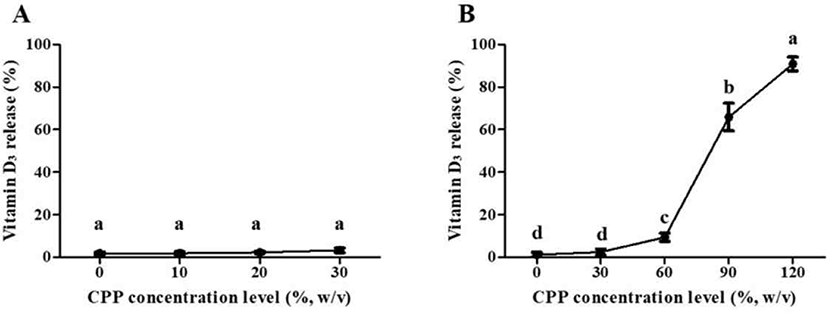
위장관 내 소화과정 중 CPP/CSO 나노 복합체 내 포집된 비타민 D의 in vitro release 평가 결과는 Fig. 6에 제시되었다. 그 결과, 위 조건(SGJ, 37°C)에서 30분간의 배양 시간 동안 유의적인 차이 없이 3% 이내의 비타민 D만이 release 되었다. 또한 CPP는 위에서 분해가 되지 않기 때문에[19] CPP/CSO 나노 복합체는 위에서의 소화과정 중 비타민 D를 효과적으로 보호할 수 있을 것으로 사료된다.
Fig. 6.
in vitro release of vitamin D from casein phosphoppeptide (CPP)/chitosan oligosaccharide (CSO) nano complexes during digestion in simulated gastric (A) and intestinal condition (B). CPP/CSO nano complexes were prepared with 0.2% (w/v) CPP solution and 0.003% (w/v) CSO solution at 5.5. Different letters on a column indicate significant differences (p<0.05).
Download Original Figure
비타민 D를 포함한 영양소 및 생리활성 물질이 흡수되는 소장 조건에서 release 측정 결과, 배양 시간이 증가함에 따라 비타민 D의 release 되는 양이 점진적으로 증가하였으며, 120분 배양 후 90.9%의 비타민 D가 release된 것을 확인하였다. 이를 통해 본 연구에서 제조한 CPP/CSO 나노 복합체는 비타민 D와 같은 생리활성물질들이 쉽게 파괴되는 위에서 이들을 효과적으로 포집 및 보호하고, 이들이 흡수되는 소장에서 release하여 소장에서 흡수되는 생리활성물질들의 효과적인 전달 시스템으로 활용될 수 있음을 규명하였다.
요 약
본 연구에서는 CPP와 CSO를 사용하여 제조한 나노 복합체의 유식품 적용성 및 포집된 생리활성물질인 비타민 D의 in vitro release를 평가하였다. 그 결과, CPP/CSO 나노 복합체는 model milk 및 model yogurt 적용 후 12일간의 저장기간 동안 높은 물리적 안정성을 지녀 식품 적용성이 뛰어남을 규명하였다. 또한 제조 공정 요인인 CPP 농도와 pH 조절을 통해 비타민 D를 90% 이상 포집할 수 있었으며, in vitro release 평가를 통해 비타민 D를 위에서 보호하고, 장에서 release 하는 나노 복합체의 특성을 규명하였다. 결론적으로 본 연구에서 제조된 CPP/CSO 나노 복합체는 뛰어난 유식품 적용성을 지닐 뿐만 아니라, 칼슘흡수 증진을 위한 비타민 D를 효과적으로 포집할 수 있으며, 포집된 비타민 D를 소장까지 안전하게 전달할 수 있는 효과적인 나노 전달체로 활용될 수 있을 것으로 기대된다.
감사의 글
이 연구는 2019년도 경상대학교 연구년제 연구교수 연구지원비에 의하여 수행되었음.
References
Baek YS, Ha HK, Lee JH, Lee MR, Lee WJ. Formation and characterization of casein phosphopeptide/chitosan oligosaccharide nanocomplex. J Milk Sci Biotechnol. 2018;36:164-170.


Cosentino S, Donida BM, Marasco E, Favero ED, Cantù L, Lombardi G, et al. Calcium ions enclosed in casein phosphopeptide aggregates are directly involved in the mineral uptake by differentiated HT-29 cells. Int Dairy J. 2010;20:770-776.


Ranaldi G, Marigliano I, Vespignani I, Perozzi G, Sambuy Y. The effect of chitosan and other polycations on tight junction permeability in the human intestinal Caco-2 cell line. J Nutr Biochem. 2002;13:157-167.


Chen LR, Wen YT, Kuo CL, Chen KH. Calcium and vitamin D supplementation on bone health: current evidence and recommendations. Int J Gerontol. 2014;8:183-188.


Hwang JY, Ha HK, Lee MR, Kim JW, Lee WJ. Manufacture and characterization of water-in-oil-in-water (W
1/O/W
2) nano multiple emulsion prepared with whey protein concentrate. J Agric Life Sci. 2014;48:301-310.


Barba FJ, Esteve MJ, Frígola A. Determination of vitamins E (
α-,
γ- and
δ-tocopherol) and D (cholecalciferol and ergocalciferol) by liquid chromatography in milk, fruit juice and vegetable beverage. Eur Food Res Technol. 2011;232:829-836.


Ha HK, Kim JW, Lee MR, Lee WJ. Formation and characterization of quercetin-loaded chitosan oligosaccharide/
β-lactoglobulin nanoparticle. Food Res Int. 2013; 52:82-90.


García-Sartal C, Romarís-Hortas V, Barciela-Alonso MDC, Moreda-Piñeiro A, Dominguez-Gonzalez R, Bermejo-Barrera P. Use of an in vitro digestion method to evaluate the bioaccessibility of arsenic in edible seaweed by inductively coupled plasma-mass spectrometry. Microchem J. 2011;98:91-96.


Lippacher A, Müller RH, Mäder K. Preparation of semisolid drug carriers for topical application based on solid lipid nanoparticles. Int J Pharm. 2001;214:9-12.


Cortés-Morales EA, Mendez-Montealvo G, Velazquez G. Polysaccharide-protein complexes as encapsulation materials: a review. Adv Colloid Interface Sci. 2021: 102398.


Lee MR, Choi HN, Ha HK, Lee WJ. Production and characterization of beta-lactoglobulin/alginate nanoemulsion containing coenzyme Q
10: impact of heat treatment and alginate concentrate. Korean J Food Sci An. 2013;33:67-74.


Ron N, Zimet P, Bargarum J, Livney YD. Beta-lactoglobulin-polysaccharide complexes as nanovehicles for hydrophobic nutraceuticals in non-fat foods and clear beverages. Int Dairy J. 2010;20:686-693.


McDonagh D, FitzGerald RJ. Production of caseinophosphopeptides (CPPs) from sodium caseinate using a range of commercial protease preparations. Int Dairy J. 1998:8;39-45.